在刚刚落幕的2023年第65届美国血液学会(ASH)大会上,中国医学科学院血液病医院安刚教授团队的多项研究入选大会报告。本期精选其中两项进行整理分享,并邀请到安刚教授进行深入解读。这两项研究中,其中一项探讨了多发性骨髓瘤(MM)低分泌进展模式对生存的影响,另一项评估了基于血液的质谱技术在MM患者病程中纵向监测M蛋白的临床应用价值。
多发性骨髓瘤低分泌进展模式预示着较差的生存率
背景
新型药物的应用大大改善了多发性骨髓瘤(MM)患者的预后。然而,大多数患者将不可避免的出现疾病疾病进展和复发。在疾病进展期(PD),很多患者会表现出明显的临床特征以及M蛋白或骨髓浆细胞(BMPC)明显升高。然而值得注意的是,在最初诊断为分泌型MM的患者中,有一个亚群表现出在疾病进展时出现较高水平的 BMPC,但同时M蛋白水平较低,这使得在不进行骨髓检查的情况下识别这一亚群具有挑战性,导致许多患者出现了进展却未得到及时治疗。对进展期分泌过少的识别和理解仍不清楚,需要进一步研究。因此,在本研究中,我们旨在根据M蛋白和BMPC比例评估疾病进展的不同模式对生存的影响,并描述亚组的特征。
方法
我们回顾性分析了本院268名MM患者在2013年1月1日至2023年7月1日期间的基线和进展临床特征。根据进展期骨髓中M蛋白和克隆性浆细胞水平的升高,我们将进展模式分为三类:a. 低分泌性进展(HypoP)是指BMPCs绝对百分比增加>10%,但血清M蛋白增加<5 g/L(或尿M蛋白增加<200 mg/24 h),诊断时为非分泌性亚型的患者除外;b. 髓外进展(EMP)是指出现新的髓外病变;c. 典型进展(ClaP)是指符合国际骨髓瘤工作组(IMWG)标准的任何一项或多项其他骨髓瘤进展标准。高肿瘤负荷指BMPC的百分比>50%。从首次复发到死亡的时间定义为首次进展后的总生存期(pro-OS)。
结果
研究共纳入了268名患者,根据他们在病情发展时的M蛋白和BMPC特征将其分组,206(76.8%)名患者被归入ClaP组,39(14.6%)名患者被归入EMP组,23(8.6%)名患者被归入HypoP组。女性在HypoP组的比例为52.2%,高于其他两组(ClaP组为36.5%,EMP组为 30.8%)。一般来说,MM患者主要为IgG亚型。有趣的是,在进展期寡分泌的患者中,M蛋白类型主要是IgA型(47.9%)和轻链型(43.5%)(P<0.001)。与ClaP组和EMP组相比,HypoP组中诊断时和疾病进展时出现 t(11;14)(36.8% vs. 16.7% vs. 11.8%)和1q21+(70% vs. 53.8% vs. 53.8%)的患者更多。在疾病进展期,HypoP组中 t(4;14)患者的比例高达50%。此外,在临床表现方面,HypoP患者在确诊时和疾病进展期更容易出现高钙血症、肾功能障碍、血清M蛋白水平降低和EMP乳酸脱氢酶(LDH)水平升高。
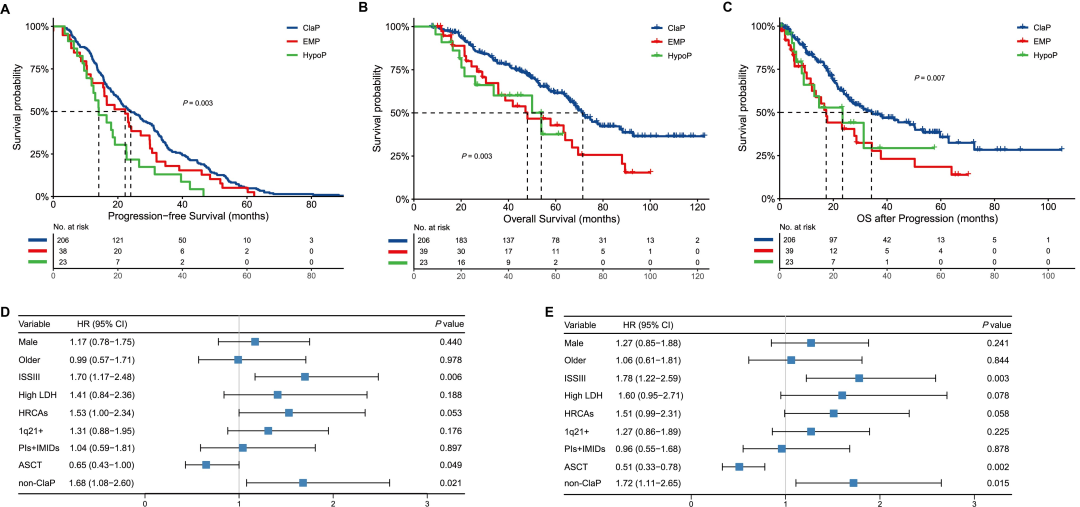
中位随访时间为 67.0个月(7.6~123.0个月)。图1展示了不同进展模式患者的无进展生存期(PFS)、OS和pro-OS。ClaP组和EMP组患者的PFS相似,而HypoP组患者的中位PFS明显较短(P=0.003,23.9 m vs. 22.6 m vs. 14.1 m)。我们还发现,具有ClaP和HypoP特征的患者中位OS(P=0.007,ClaP vs. EMP vs. HypoP为71.4 m vs. 48.0 m vs. 53.9 m)和pro-OS(P=0.012,ClaP vs. EMP vs. HypoP为34.2 m vs. 17.3 m vs. 23.4 m)均较差。我们将这两种情况总称为非ClaP。在Cox-回归中,多变量分析显示ISS-III、ASCT和非ClaP与较短的pro-OS和OS相关(下图)。
专家解读
MM 仍无法治愈,大多数MM患者最终都会复发。已有回顾性研究关注不同复发模式[包括临床进展(CP)和生化进展(BP)]的意义,这些研究揭示了CP与BP相比生存预后较差之间的关联。
然而,除了有或无临床特征时,PD患者有时会出现不同水平的M蛋白和BMPC,但很少有研究对此进行关注。一些研究人员发现,在少数病例中,M蛋白存在一种独特的现象,称为轻链(LC)逸出或非分泌性逸出(NS),即M蛋白分泌从完整的免疫球蛋白(Ig)转变为仅分泌LC或失去分泌原有M蛋白的能力,LC和NS逃逸的预后价值仍不明确。
我们的研究首次结合了M蛋白和BMPC的变化趋势来探讨其进展模式。数据显示,在所有帕金森病患者中,具有少分泌特征和BMPC水平显著升高的患者约占8.6%,而M蛋白并没有像LC逃逸现象一样转变为其他类型。在确诊时,寡分泌型MM的发病率低于10%,而且该亚组患者倾向于出现侵袭性临床表现,如高钙血症和肾功能障碍,并伴有高危遗传学异常。与寡分泌/不分泌型MM诊断时的预后价值不确定不同,BMPC水平升高导致的低分泌会带来不良预后。此外与其他研究结果类似,我们的数据也显示,EMP患者的肿瘤负荷较高,生存期较短。
总之,M蛋白的明显升高、新的或扩大的髓外病变以及明显的临床表现都是判断疾病进展的指标。然而,需要注意的是,分泌型疾病患者在病程中可能仅表现为轻度或无M蛋白水平升高,这并不一定意味着患者病情稳定或获得缓解,尤其是诊断时有侵袭性临床表现或HRCA的患者。在这种情况下,骨髓检测在识别和检测这一特殊群体方面起着至关重要的作用。具有EMP或HypoP特征的患者往往预后较差,因此,尽早识别这些特殊患者并加强治疗策略非常重要。
多发性骨髓瘤患者微小残留病血清M蛋白质谱检测
研究介绍
这项壁报展示了我们团队进行的一项回顾性的真实世界研究,以评估基于血液的质谱技术在多发性骨髓瘤(MM)患者病程中纵向监测M蛋白的临床应用价值。采用克隆多肽质谱法(EasyMMS)分析56例MM患者的连续血清样本,将质谱结果与血清免疫发射电泳(IFE)、多参数流式细胞术(MFC)和二代流式细胞术(NGF)测定的结果进行比较,以确定不同疾病监测方案之间的一致性。
56名MM患者中,38名IgG型MP患者可通过质谱分析进一步确定IgG亚型。使用IFE对基于血液的MS-MRD与传统的M蛋白诊断方法的性能进行了初步比较。在相似时间点采集的397个可比较结果中,70.8%(281/397)的样本既是M-MRD阳性样本,又是IFE阳性样本;3.3%(13/397)的样本既是MS-MRD阴性样本,又是IFE阴性样本;25.7%(102/397)的样本既是MS-MRD阳性样本,又是IFE阴性样本。与MFC和NGF相比,MS-MRD的敏感度为100.0%,特异度分别为1.9%和22.2%。考虑到EasyM在dotp>0.9的临界值下具有极高的灵敏度,我们将NGF的灵敏度作为检测标准(即检测灵敏度≤10),并通过ROC分析设定EasyM MS阴性临界值,确定为<初诊的1.86%。EasyM的灵敏度与IFE(88.3%)、MFC(85.1%)和NGF(93.2%)相比仍然很高,特异度也大大提高,分别为90.4%、55.8%和93.2%。
根据患者是否达到MS-MRD阴性将其分为MS阳性组和MS阴性组,并计算各组的中位PFS和OS。MS阳性组和MS阴性组的中位PFS分别为20.6个月和61.8个月。MS阳性组的中位OS为55.7个月,MS阴性组的中位OS未达到(NR),MS阴性组的mPFS和mOS均明显长于MS阳性组(P<0.001)。EasyM具有高灵敏度和微创的技术优势,在疗效评估和预后评估方面也具有重要意义。未来,EasyMMS检测可作为一种基于外周血的微创MRD监测方法应用于临床。
专家解读
MRD监测在多发性骨髓瘤的临床管理中具有举足轻重的作用,理想状态下通过序贯监测MRD,能给临床医生提供实时信息。传统的MRD检测主要包括多参数流式(MFC)、二代流式(NGF)和二代测序(NGS),但这些检测方式都需要对患者进行有创骨髓穿刺,既不方便频繁采样,也增加患者的检测痛苦和检测风险。此外,由于浆细胞在骨髓中呈灶状分布,以及存在骨髓液稀释等问题,骨髓MRD评估存在假阴性。
M蛋白作为浆细胞分泌的产物,在血液中呈均一分布,是理想的“血清肿瘤标记物”。但针对M蛋白的血清蛋白电泳和免疫固定电泳存在检测灵敏度较低的缺陷,因而无法在深度缓解的患者中进一步区分患者疗效。蛋白质谱具有高度检测灵敏度,利用不同MM患者之前M蛋白的序列差异,可以实现微创和高灵敏度监测患者M蛋白,可以实现对完全缓解(CR)阶段的MM患者进行频繁的MRD动态序列定量监测,从而对药物治疗深度和有效性进行客观科学的评估,有效监测疾病的复发并指导临床诊疗规范服务。EasyM™是一种克隆特征肽质谱检测方法,可以实现靶向定量监测患者M蛋白水平,我们通过对比同一时间点外周血M蛋白的EasyM监测结果以及骨髓中MRD评估结果,发现EasyM可以达到10-5检测灵敏度,其检测结果具有预后评估价值,亦可成为评估MRD状态作为新型治疗药物临床试验的疗效终点的理想检测方法,相较于现有临床使用的有创骨髓穿刺的血检方法,EasyM™采取的无创血检既减少了对患者造成痛苦的风险,其灵敏度也显著提高,具有广泛的市场应用前景。