编者按:欧洲血液协会(EHA)年会作为血液领域的国际会议,汇聚了全球众多专家学者,旨在共同分享并深入探讨血液领域的创新理念及科学与临床研究进展,推动血液领域的持续发展。在本届大会上,脾酪氨酸激酶(SYK)抑制剂的研究成果受到了关注。索乐匹尼布(HMPL-523)作为中国首款(*截至发稿日)申报上市的国产SYK抑制剂,在本届EHA会议中公布了多项研究的结果。《肿瘤瞭望-血液时讯》本期特邀昆明医科大学第二附属医院周泽平教授解读索乐匹尼布在原发免疫性血小板减少症(ITP)领域的ESLIM-01研究(NCT05029635)内容,以期为临床实践提供参考。
辨析ITP治疗药物机制差异
《肿瘤瞭望-血液时讯》:请问与TPO/TPO-RA等现有的治疗手段相比,ESLIM-01研究中的SYK抑制剂索乐匹尼布在作用机制上有哪些差异?
周泽平教授:索乐匹尼布作为一种选择性的口服SYK抑制剂,通过抑制SYK活性,干扰B细胞受体与Fc受体的信号传导,进而减弱免疫反应。特别是针对B细胞和巨噬细胞1、2,索乐匹尼布展现出了双重作用机制。
SYK抑制剂与血小板生成素/促血小板生成素受体激动剂(TPO/TPO-RA)机制有所区别,TPO/TPO-RA主要模拟或强化TPO的作用,以促进血小板的生成。具体来说,TPO通过与TPO受体(c-MPL)结合,促进骨髓中巨核细胞的分化和成熟,进而增强血小板的生成;而TPO-RA则通过激活c-MPL,直接刺激骨髓内巨核细胞,从而产生更多的血小板3、4。由于TPO/TPO-RA的上述机制,使得它们能快速增加血小板的生成,应用后血小板计数会迅速上升,可能导致PLT曲线的较大波动。SYK抑制剂并不直接刺激血小板的生成。它通过抑制免疫系统中B细胞和Fc受体的信号传导,减少了抗体介导的血小板破坏,从而逐步提升血小板计数,因此索乐匹尼布治疗的PLT曲线表现相对平稳5。
利妥昔单抗等抗CD20抗体则主要通过与B细胞表面的CD20分子结合,介导B细胞的凋亡和清除。鉴于B细胞是产生抗体的主要细胞类型,因此减少B细胞数量能降低自身抗体的产生,从而减少血小板破坏。而SYK抑制剂则直接作用于免疫信号通路,特异性较高,对B细胞和巨噬细胞产生作用,减少血小板损失,提高血小板计数。与广泛的免疫抑制相比,SYK抑制剂对免疫系统的整体抑制作用较小。
此外,在ITP治疗中,SYK抑制剂与抗CD20单抗的起效速度有所不同。SYK抑制剂基于其直接抑制B细胞和巨噬细胞的活化,研究中展现出或可快速减少血小板破坏的作用。抗CD20抗体治疗ITP的反应时间存在个体差异,部分患者在4周内可见血小板计数增加,而一些患者可能需要3个月的治疗达到正常值6。ESLIM-01研究显示,索乐匹尼布能在1周左右(8天)使血小板计数达到或超过50×10⁹/L5。
ESLIM-01研究设计及结果介绍
《肿瘤瞭望-血液时讯》:在本次EHA 2024大会上,基于索乐匹尼布创新机制所开展的ESLIM-01研究的结果已正式公布。请您介绍一下这项研究的设计及主要结果。
周泽平教授:ESLIM-01研究的入组条件设定为5:成人ITP患者需接受过至少一种治疗方案,且允许接受一种ITP维持治疗,病程超过12个月。研究采用的治疗方案为索乐匹尼布或安慰剂。主要的研究终点聚焦于持续应答率,即在14-24周的6次访视中,在无紧急治疗干预下患者需至少达到4次血小板计数不低于50×10⁹/L。次要终点则包括总体应答率,定义为在无紧急治疗干预下至少有一次血小板计数达到或超过50×10⁹/L,同时还涵盖应答时间、基线时紧急治疗的频率、伴随使用的抗ITP药物的减少情况、WHO出血评分以及基于SF-36的生活质量评估结果。
ESLIM-01研究已达成主要及所有次要终点,取得了相应的成果5。首先,索乐匹尼布中位8天即可使血小板计数提升至50×10⁹/L。
其次,索乐匹尼布的整体应答率达71%,对照组为16%。在索乐匹尼布治疗组中,血小板计数中位范围稳定在(50~90)×10⁹/L。此外,索乐匹尼布的治疗效应应答平稳,持续应答率达到48%,持续有效患者的血小板计数中位范围保持在(80~100)×10⁹/L。
此外,索乐匹尼布在降低出血风险方面呈现出的研究结果良好。与安慰剂组相比,治疗12周和24周时,WHO出血评分的改善具有统计学意义(P=0.0002)。最后,研究提示了索乐匹尼布在改善患者的生活质量的潜在作用,包括生理功能、疲劳状态及总体健康情况等方面。
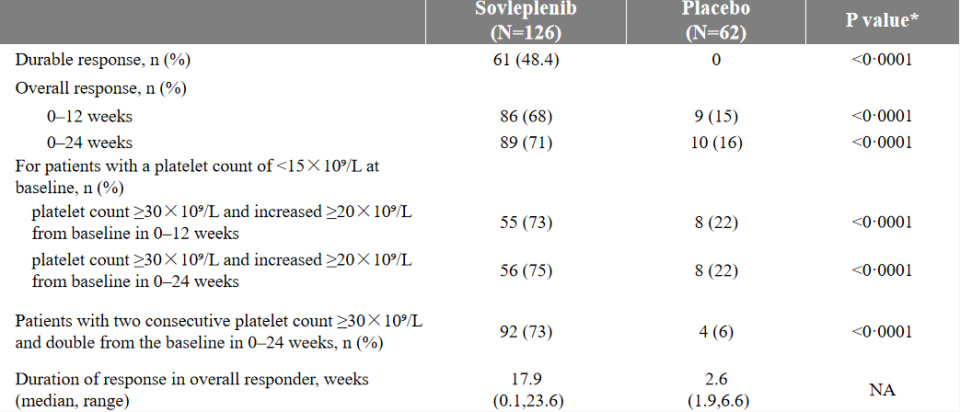
主要终点和关键次要终点5
剖析研究中索乐匹尼布总体安全性表现
《肿瘤瞭望-血液时讯》:药物机制与安全性表现同样相关,能否请您详细解析ESLIM-01研究中索乐匹尼布的安全性数据?在实际临床应用中,医生们通常会特别关注感染、肝功能异常和血栓等不良事件的发生风险,在这些方面索乐匹尼布表现如何?
周泽平教授:在深入分析ESLIM-01研究的安全性数据5之前,我们需明确此研究是在全球新冠疫情大规模流行这一独特背景下进行的。此外,鉴于安慰剂在试验期间未显示疗效,因此,绝大部分接受安慰剂治疗的无应答患者在第12周时便提前出组。基于上述前提,索乐匹尼布组的药物暴露时间达到了对照组的两倍(24.1周 vs. 12.1周)。尽管暴露时间增加,索乐匹尼布组≥3级治疗期间出现的不良事件(TEAEs)(25.4% vs. 24.2%)和严重TEAEs(20.6% vs.17.7%)的发生率与安慰剂组相当,且截至分析时未出现死亡病例。

总体安全性情况5
在ESLIM-01研究中,TEAEs包括上呼吸道感染(29%)和COVID-19感染(24%)等。这一现象可能与SYK抑制剂的作用机制相关,免疫抑制会增加感染的风险7。研究数据表明,与感染相关的TEAEs发生率未超过30%,且≥3级为1%~2%。在实际临床应用中,建议临床医生密切监测患者情况,以便尽可能有效预防和管理潜在的感染风险。
在所有级别的TEAEs中,24%的患者出现了血乳酸脱氢酶(LDH)的升高,另有15%的患者观察到谷丙转氨酶(ALT)的升高。这些生化指标的升高可能表明肝功能损伤,但研究中无≥3级的严重不良事件。LDH与ALT的升高往往标志着肝细胞损伤或破坏,这可能是由于SYK抑制剂药物代谢对肝脏的影响以及免疫介导的肝脏细胞损伤有关。因此,建议医生持续监测患者的肝功能指标,以便及时发现并妥善处理相关潜在的问题。
血小板计数的波动与血栓风险之间存在一定的关联性8,ESLIM-01研究中未观察到到血栓栓塞事件的发生。综合前述的索乐匹尼布机制和研究结果,其血小板计数呈现较稳定的增加趋势,或可提示其不易引起急剧的血液动力学变化,从而显著增加血栓风险。此外,索乐匹尼布的胃肠道毒性和高血压发生率也较低。总体而言,根据ESLIM-01研究的数据,索乐匹尼布在治疗ITP方面展现出了良好的安全性。
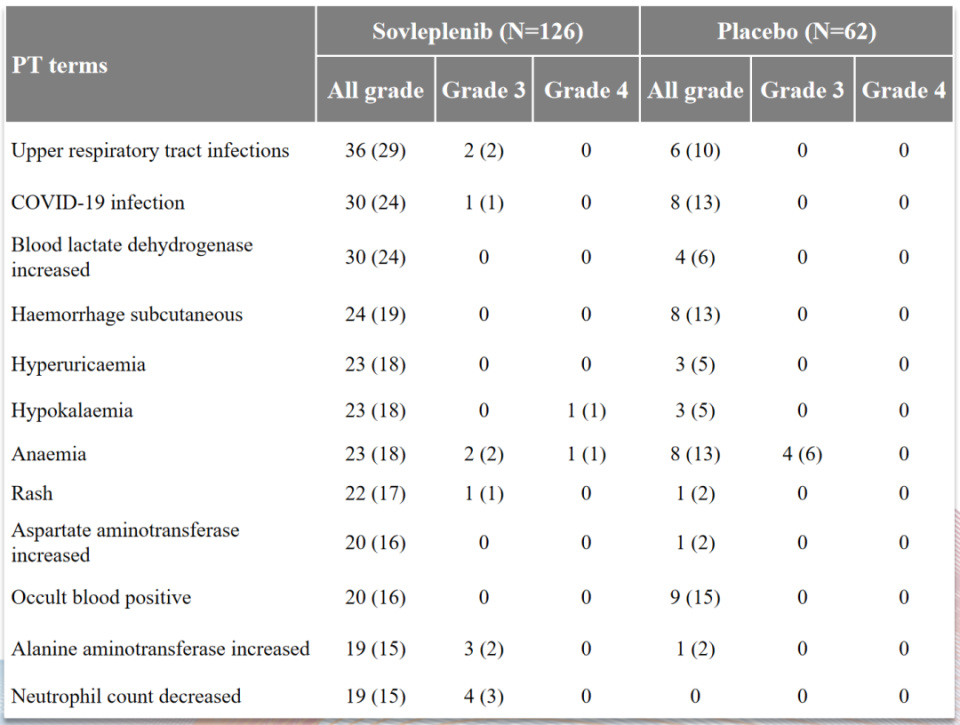
常见TEAEs情况5
*索乐匹尼布组中2例4级不良事件与索乐匹尼布治疗不相关
研究次要终点的结果分享
《肿瘤瞭望-血液时讯》:在ESLIM-01研究中,还关注了紧急治疗、WHO出血评分和生活质量等次要终点。能否您分享一下索乐匹尼布在这些方面的结果?
周泽平教授:治疗ITP的核心目标在于提升血小板数量,并尽可能降低出血风险。除了疗效和安全性的数据提示未来索乐匹尼布或可成为成人ITP患者的治疗选择外,在ESLIM-01研究中还探索了一些次要终点。例如,索乐匹尼布组在紧急治疗需求上有所降低(22% vs. 35%)5,显示索乐匹尼布在改善病情、减少额外治疗需求方面的潜在作用。WHO出血评分的平均值在12周和24周时均有所下降(0.56 vs. 0.79)5,意味着出血的严重程度和频率得到了一定控制。此外,索乐匹尼布还减少了抗ITP药物的剂量(27% vs. 10%)5,或可帮助降低药物副作用的风险,简化治疗方案,有望对患者的长期管理和生活质量产生积极影响。
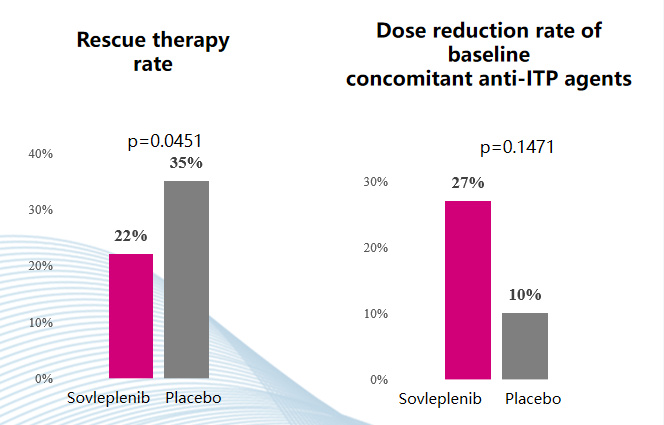
紧急治疗与抗ITP药物减量情况5
在生活质量情况方面,基于SF-36量表的评估,与基线相比,索乐匹尼布组患者的躯体功能、因情绪问题导致的角色限制、体能/疲劳状况、总体健康、因躯体健康导致的角色限制、情绪健康和社会功能等方面的评分均有所改善,显示索乐匹尼布治疗对患者的日常生活和心理状态产生了一定积极影响,有望帮助提升患者的社会参与度。
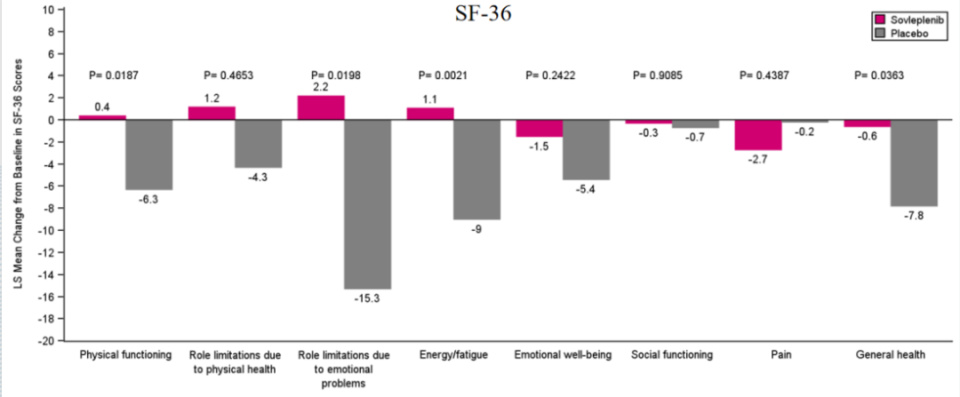
生活质量情况5
患者依从性及治疗管理
《肿瘤瞭望-血液时讯》:在用药方式的便捷性以及对不同患者群体的适用性等方面,您如何看待索乐匹尼布对提高患者依从性以及治疗管理的潜在影响?
周泽平教授:索乐匹尼布采用每日一次的口服给药方式,这一用药模式或可以提升患者的依从性,用药便利性可助于改善患者的治疗体验。良好的依从性是实现治疗效果的关键之一,有助于患者持续获得药物的治疗效益。
此外,索乐匹尼布无需剂量调整,一定程度上简化了治疗流程。对于患者而言,减少了定期血液监测和剂量调整的操作,降低了医疗访视的频率和治疗的复杂性。此外,这种服药方式易于老年患者理解和遵循,对于需要长期管理的慢性病患者较为友好,有助于他们更好地将治疗融入日常生活。索乐匹尼布在相关研究中尚未特别指出与特定食品的相互作用,因此,这可能表明患者在接受治疗期间无需特别调整饮食习惯。
综上所述,索乐匹尼布在用药方式、便捷性、适用性以及患者依从性等方面展现出的特性相互交织,有望共同对治疗ITP的总体效果增添助力,期待未来可以为ITP患者提供一个新的治疗选项。
专家简介
周泽平 教授
博士,博导,博士后导师
昆明医科大学第二附属医院血液科主任
国家卫健委儿童血液病、恶性肿瘤专家委员会分会副主委
中国老年保健协会肿瘤免疫治疗专委会副主任委员
中国医师协会血液科医师分会常委,云南省主委
中国抗癌协会淋巴瘤专委会常委,云南省主委
云南省医学会血液学分会副主任委员
中国血液病专科联盟再障协作组副组长
云南省中青年学术及技术带头人、领军人才、名医、省贴
主持国家自然科学基金6项
发表论文87篇(BJH、Haemophilia、TR等SCI: 40)
《Journal of Immunology Research》编委
《中华血液学杂志》通讯编委、《血栓与止血杂志》常务编委
《肿瘤药学》、《中国肿瘤临床与康复》编委
参考文献:
1. Cai Y, He J, Wu Z, He W, Dai X, Xu Y, Cheng M, Yang N, Ren Y, Wang G, Wang J, Sai Y, Jia H, Dai G, Li X, Su W. Preclinical Pharmacology Characterization of Sovleplenib (HMPL-523), an Orally Available SYK Inhibitor. J Pharmacol Exp Ther. 2024 Jan 2;388(1):156-170.
2. Adapted from cines DB, Blanchette vs.N Engl J Med. 2002,346(13): 995-1008.
3. 中国医院协会, 中国医疗保健国际交流促进会, 中国药学会医院药学专业委员会. 促血小板生成药物临床应用管理中国专家共识(2023年版)[J]. 中国医院用药评价与分析, 2023, 23(4): 349-354.
4. 张蕾, 李莉, 王琳, 等. 血小板生成素的研究新进展[J]. 生物技术通讯, 2022, 23(6): 1242-1246.
5. Renchi Yang, et al. Efficacy and safety of the Syk inhibitor sovleplenib (HMPL-523) in adult patients with chronic primary immune thrombocytopenia in China (ESLIM-01): a randomized, double-blind, placebo-controlled phase 3 study. 2024 EHA:Abstract S316
6. Neunert, C. E., Terrell, D. R., El-Harake, W. A., & Vesely, S. K. (2010). The American Society of Hematology 2010 evidence-based practice guideline for immune thrombocytopenia. Blood, 116(23), e407-e415.
7. Connell, N. T., Berliner, N., & Nathan, T. (2019). Fostamatinib for the treatment of chronic immune thrombocytopenia. Blood, 133(19), 2027-2030.
8. Rinder, H. M., Schuster, J. E., Rinder, C. S., Wang, C., Schweidler, H. J., & Smith, B. R. (1998). Correlation of Thrombosis With Increased Platelet Turnover in Thrombocytosis. Blood, 91(4), 1288-1294.
NP-SOV-24N951-Valid Until-2026-July
本资料由和黄医药提供支持。
本资料旨在促进医药信息的沟通和交流,而非广告宣传。