7月20日,第五届淋巴瘤&骨髓瘤免疫与靶向治疗大会暨高博医学学术会议在北京顺利召开。大会以“精准、整合、创新”为核心理念,内容紧密追踪29届欧洲血液学协会年会(EHA 2024)和2024年美国临床肿瘤学会(ASCO)年会的最新进展和前沿议题。为深化交流与探讨,《肿瘤瞭望-血液时讯》特别邀请北京积水潭医院鲍立教授进行专访,探讨领域进展,分享学术洞见。
《肿瘤瞭望-血液时讯》:噬血细胞综合征是一种遗传性或获得性免疫调节功能异常导致的严重炎症反应综合征,临床上诊断的难度相对较大,容易误诊和漏诊,首先请您谈一谈HLH目前的临床诊断路径应如何实施?
鲍立教授:噬血细胞综合征(HPS),亦名噬血细胞性淋巴组织细胞增多症(HLH),是一种由遗传性或获得性免疫调节功能异常引发的严重炎症反应综合征。其主要临床特征包括发热、血细胞减少、肝脾肿大,以及在肝、脾、淋巴结和骨髓组织中发现噬血现象。目前,HLH的诊断标准广泛采纳的是国际组织细胞协会在2004年进行的修订版本。当符合以下任一条件时,即可诊断为HLH:首先,分子诊断显示与HLH相符,即存在已知的HLH相关致病基因,例如PRF1、UNC13D、STX11、STXBP2、Rab27a、LYST、SH2D1A、BIRC4、ITK、AP3β1、MAGT1、CD27等基因的病理性突变;其次,符合以下8项指标中的至少5项:①发热:体温>38.5 ℃,持续>7 天;②脾大;③血细胞减少(累及外周血两系或三系):血红蛋白<90 g/L(<4周婴儿,血红蛋白<100 g/L),血小板<100×109/L,中性粒细胞<1.0×109/L 且非骨髓造血功能减低所致;④高甘油三酯(triglyceride,TG)血症和(或)低纤维蛋白原血症:甘油三酯>3 mmol/L或高于同年龄的3个标准差,纤维蛋白原<1.5 g/L或低于同年龄的3个标准差;⑤在骨髓、脾脏、肝脏或淋巴结中发现噬血现象;⑥NK细胞活性降低或缺如;⑦血清铁蛋白升高:铁蛋白≥500 μg/L;⑧sCD25(可溶性白细胞介素‑2受体)升高。
尽管当前对于该疾病已确立了一套明确的诊断标准,但核心的临床挑战仍在于其发病机制的解析。举例来说,若患者表现出发热、脾肿大以及两系或三系血细胞减少的症状,并且伴随铁蛋白水平升高、高甘油三酯血症或低纤维蛋白原等指标的异常,则基本符合该疾病的五项诊断标准,诊断流程相对清晰。然而,在临床实践中,更为关键的是探究导致HLH的根本原因,包括是否存在感染、免疫性疾病或血液恶性肿瘤等继发性因素,或是否为原发性疾病。
继发性HLH是一种由肿瘤、风湿免疫性疾病、感染等多种因素诱发的严重炎症反应综合征。对于当前无法检测到已知HLH致病基因,且无法明确继发病因的患者,则暂时将其归类为原因不明的HLH,在后续的治疗和随诊过程中,仍需持续寻找其原发的病因。而原发性HLH则是由遗传性淋巴细胞毒功能受损或炎症、活性相关基因缺陷所导致,其类别涵盖家族性HLH、免疫缺陷综合征相关HLH、X连锁淋巴增生性疾病以及EB病毒驱动型HLH。
现有指南和路径为临床医生提供了明确的诊断框架,使得在面对复杂且多样化的临床表现时,能够有条不紊地进行诊断流程,确保每一个疑似病例都能得到细致、全面的评估。遵循规范化的指南和明确的临床诊断路径,在诊断HLH时,可以有效地降低误诊和漏诊的风险,进而显著提升诊断的准确性和效率。通过规范化流程,临床医生们可以快速识别并聚集关键的诊断信息,包括患者的病史、家族史、临床症状以及必要的实验室和影像学检查结果。这不仅有助于提高首次诊断的准确性,减少了不必要的重复检查和治疗延误,而且能够为患者提供更及时、更有效的治疗方案,从而改善他们的预后。因此,标准化诊断流程的运用对于提升HLH的整体诊疗水平具有重要意义。
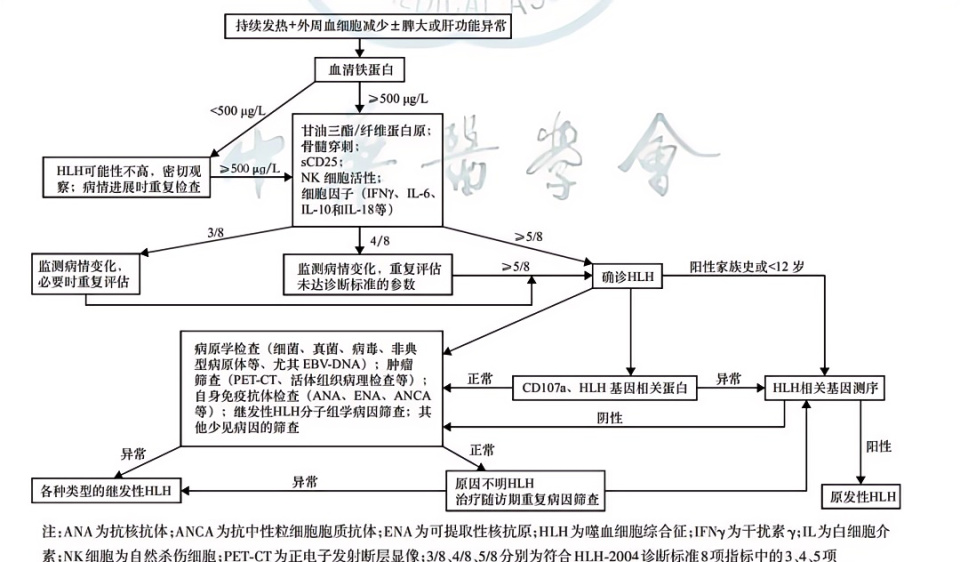
HLH诊断路径
《肿瘤瞭望-血液时讯》在明确HLH诊断后,请您谈一谈目前指南推荐的一线和挽救治疗策略?近年来HLH治疗的重要进展有哪些?
鲍立教授:在治疗之前,首要步骤是明确HLH的诊断,并随后确定其病因。鉴于不同病因对治疗策略的影响,临床医生需要为每位患者制定个性化的治疗方案。例如,对于非遗传性及病因不明的HLH患者,激素和丙球可能是合适的治疗选择。若病因是病毒感染,如EB病毒感染,治疗方案需根据病毒感染的细胞类型(如T细胞或B细胞)进行调整。若病因是淋巴瘤,则可能采用HLH-94方案联合化疗。对于风湿免疫性疾病导致的HLH,则推荐采用大剂量激素治疗原发病。
在过往的治疗实践中,HLH-94方案(依托泊苷+地塞米松)被广泛采用作为治疗方案,发挥了重要的作用。然而,随着医学研究的不断深入和进展,近年来,逐渐发现JAK通路抑制剂芦可替尼在治疗HLH方面具有显著的疗效。这种新的治疗方法的优势在于,患者可以通过口服给药的方式进行治疗,而且只需要较小的剂量,就能够达到令人满意的治疗效果。这一突破性的进展为患者带来了福音,意味着他们可以避免因化疗带来的痛苦和不适。总的来说,芦可替尼等新型治疗药物,凭借其独特的给药机制以及显著的治疗效果,正逐步重塑HLH的治疗领域,引领着治疗格局的深刻变革。
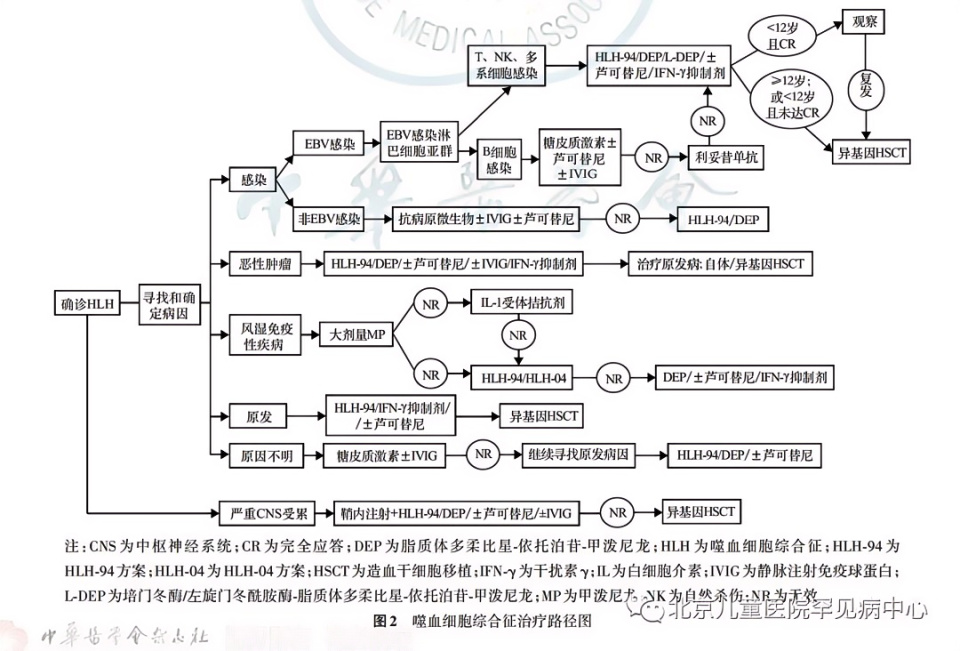
HLH治疗路径
《肿瘤瞭望-血液时讯》:CAR-T细胞输注相关的噬血样综合征在患者群体和CAR-T细胞构建体中广泛发生,在此能否请您谈一谈这类HLH的严重程度分级和临床治疗策略?
鲍立教授:在CAR-T治疗之后,患者可能会面临多种合并症,其中包括细胞因子释放综合征(CRS)和免疫效应细胞相关神经毒性综合征(ICANS)等。值得注意的是,CAR-T治疗后发生的噬血细胞性淋巴组织细胞增生症/巨噬细胞活化综合征(HLH/MAS)被单独分类,其特点在于巨噬细胞和淋巴细胞的异常活化,炎性细胞因子的显著升高,淋巴细胞的组织浸润以及免疫介导的多器官功能衰竭。因此,针对此类病症的治疗策略需同时考虑HLH的缓解以及CAR-T治疗后炎症反应的调控。在此情况下,激素、托珠单抗等药物的应用被视为合适的治疗选择,而联合使用芦可替尼可能会进一步提升治疗效果。
CRS的分级体系共包含4级:1级CRS可能仅表现为发热等轻度炎症反应,而无血流动力学变化。当CRS进展至2级时,可能伴随轻度的低血压和低氧血症,此时可能需要采用托珠单抗或激素进行治疗。3级CRS则表现为低血压和低氧血症的进一步加重,可能需要高流量给氧甚至升压药物的干预。而4级CRS则可能涉及机械通气等更为复杂的治疗手段。因此,治疗策略需根据CRS的严重程度进行阶梯式调整。当CAR-T治疗后出现明确的HLH转化迹象时,除了激素、托珠单抗等药物外,应尽快给予芦可替尼治疗,并结合其他更为有力的对症治疗措施,以确保患者得到及时有效的治疗。
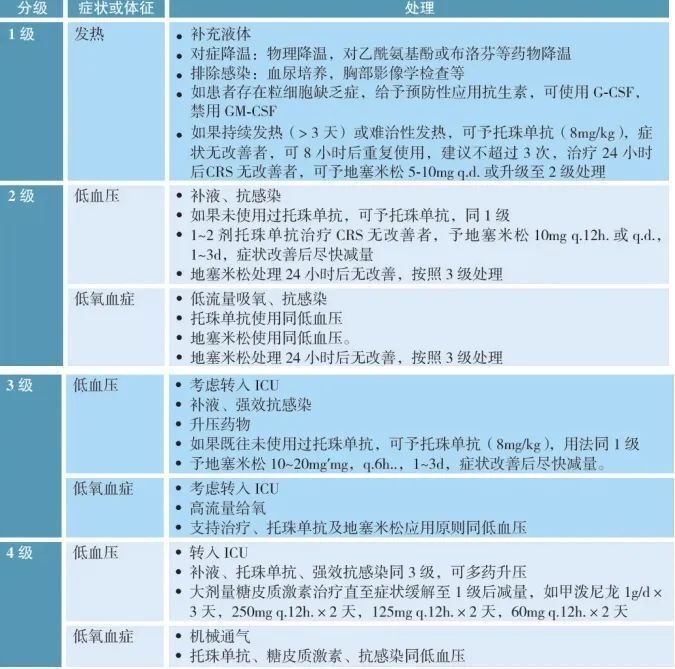
CRS分级及处理
专家简介
鲍立 教授
首都医科大学附属北京积水潭医院血液科主任、主任医师
中国医药教育协会转化医学专业委员会 主任委员
北京围手术期医学研究会血液专业委员会 主任委员
北京慢性病防治与健康教育研究会血液病学专业委员会 主任委员
北京市科委医疗卫生领域专家库成员