2024年8月24日,第十二届陆道培血液病学术论坛圆满落下帷幕。会上,来自陆道培医院赵艳丽教授带来了主题为《异基因移植治疗原发性骨髓纤维化》的精彩报告,围绕欧洲血液与骨髓移植学会(EBMT)/欧洲白血病网络 (ELN) 2024年骨髓纤维化移植专家共识,对移植的适应证、时机、供者选择、预处理方案,以及芦可替尼在移植前后的应用进行了深入阐述。现《肿瘤瞭望-血液时讯》特将报告精要整理成文,以飨读者。
PMF患者预后评估
不同的骨髓增殖性疾病预后不同,例如原发性骨髓纤维化(PMF)的中位生存时间仅有4.4年,而真性红细胞增多症(PV)和原发性血小板增多症(ET)分别为15年和18年。因此对骨髓纤维化病人进行危险分层十分重要。
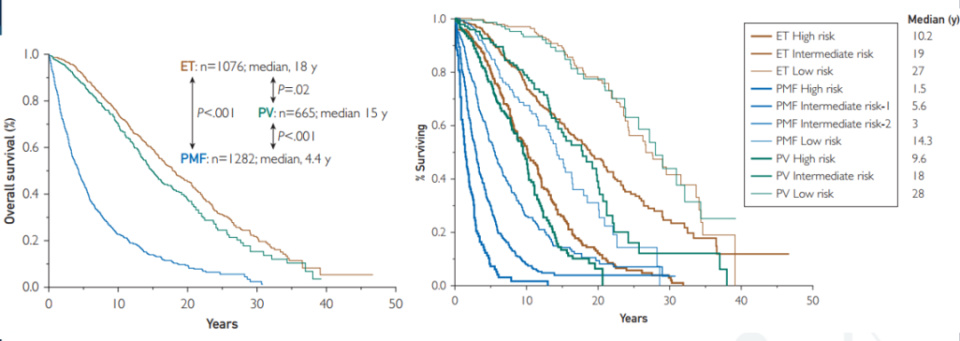
图1. 不同类型骨髓增殖性疾病预后差异
PMF的评分系统发展已较为完善,主要有以临床特征和实验室结果为依据的国际预后积分系统(IPSS)和动态国际预后积分系统(DIPSS),以及在此基础上添加了细胞遗传学诊断的DIPSS-Plus,随着分子生物学的发展相继演化出了突变强化国际预后评分系统(MIPSS-70)、MIPSS70-Plus、继发性骨髓纤维化预后模型(MYSEC-PM)、MPN Multistage评分,以及后期单纯以遗传学为依据的遗传学驱动预后评分系统(GIPSS)评分。
目前已知与PMF预后相关的基因突变有ASXL1、SRSF2、EZH2、IDH1/2及U2AF1,出现≥2种突变即可认为是高危的分子学标志,也可作为异基因移植的适应证。在当前医学领域的发展进程中,遗传学与分子生物学的地位日益凸显,其对于疾病诊断、治疗策略制定及预后评估的深远影响不容忽视。鉴于这一现状,建议临床实践中广泛采纳并应用最新的评分系统,以确保对患者病情及预后进行更为精确、科学的评估。
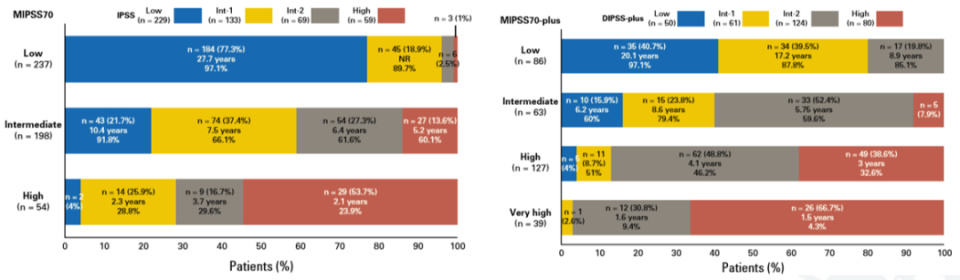
图2. PMF的预后分层
PMF患者移植适应证和时机
据EMBT统计的骨髓纤维化异基因移植数据显示,自1995年至2018年的二十三年间,全球范围内实施的移植手术例数呈现稳步增长的态势。在此期间,接受移植治疗的患者群体特征发生了一系列显著变化:患者的中位年龄从49岁上升至59岁;Karnofsky功能状态(KPS)评分低于90分的患者比例有所上升;供体选择方面,非血缘全相合供者数量逐年增加;在预处理方案的调整上,传统的清髓性方案(MAC)预处理应用有所减少,而采用白消安(Bu)-为基础的预处理方案及抗胸腺细胞球蛋白(ATG)的应用则显著增加;急性移植物抗宿主病(GVHD)及慢性GVHD的发生率则呈现出下降趋势。
异基因移植适应证详见表1。此外,患者意愿、疾病特点(如TP53突变)以及患者特点(体能状态、同胞相合供者)也是需要考虑的状态。移植时机方面,根据最新EBMT和欧洲白血病网络(ELN)推荐,高危及中危-2应立即移植,中危-1可择期移植;接受芦可替尼治疗的患者需要及时评估疗效,6个月的治疗反应(RR6)高危组患者需要移植。

表1. 异基因移植的适应证
脾脏增大患者的移植前治疗
脾脏大于15cm的患者,移植前脾切除可以显著降低非复发死亡(NRM),复发率增加不显著。
脾脏肋缘下<5cm者直接移植;
脾脏肋缘下≥5cm或有脾大相关症状者最理想的治疗是JAK抑制剂;
脾脏肋缘下≥15cm者可尝试其他JAK抑制剂、新型药物、脾切除、脾区放疗等;
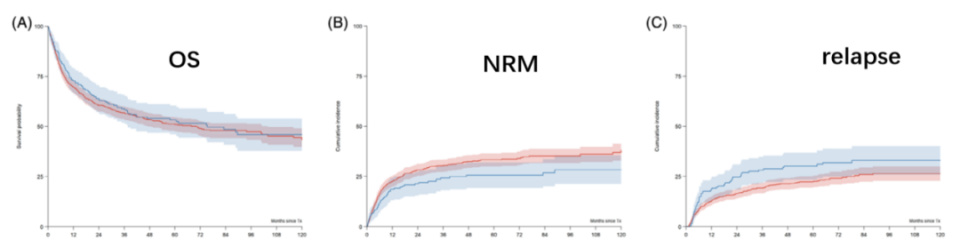
图3:脾切对移植结果的影响(红色:未脾切,蓝色:脾切)
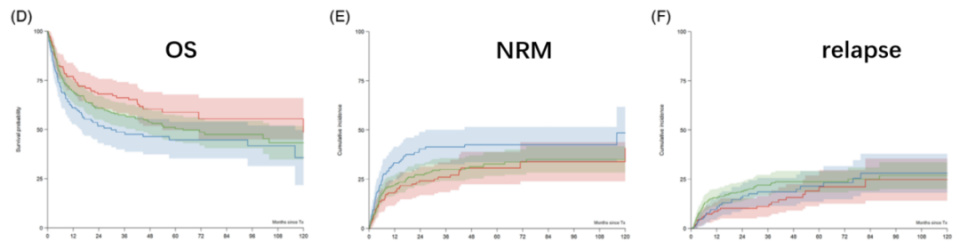
图4. 脾脏大小和切脾对移植结果的影响(红色:<5cm,绿色:5~14cm,蓝色:>15cm)
移植前后的管理
同胞相合供者仍然是最首选的供者类型,无论是同胞相合及非血缘移植还是半相同及移植后环磷酰胺(PTCY),均推荐外周血干细胞移植。同胞相合及非血缘移植选择高剂量干细胞输注(CD34+ >7.0×106/kg)。
预处理方面,临床实践中越来越多医生选择减低强度的预处理方案,对总体的生存率没有影响。
移植前应用芦可替尼的患者生存率没有明显差异,移植后应用芦可替尼作为维持治疗预防复发的证据不足。
多打击TP53突变是骨髓纤维化移植的极高危因素,单打击TP53突变与无TP53突变结果相似。
抗人T细胞兔免疫球蛋白(ATLG)能够提升移植后的无复发无排异生存率(GRFS),在临床应用中愈发广泛。肥胖对移植结果的影响并不显著,但移植6个月内体重快速下降(降低>10%)与更高的移植后死亡率相关,且与更短的生存期相关。
加速期/急变期PMF的治疗
符合移植指征的加速期或急变期PMF患者应尽量进行移植,不符合指征者可使用维奈克拉联合去甲基化药物等治疗争取缓解。
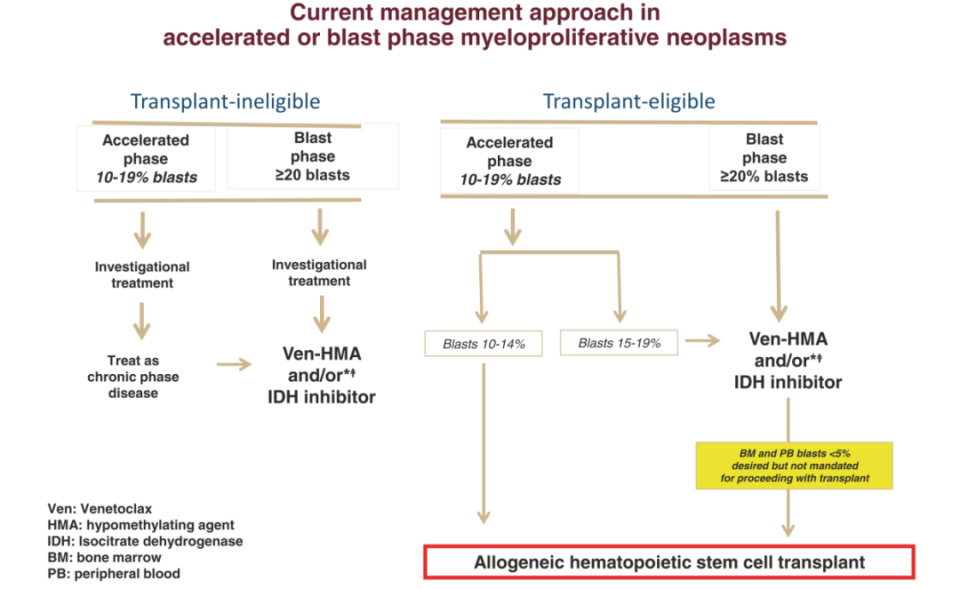
图5. 加速期或急性期PMF的治疗方法
急变期PMF患者在髓系肿瘤中预后最差,长期生存率低于20%。
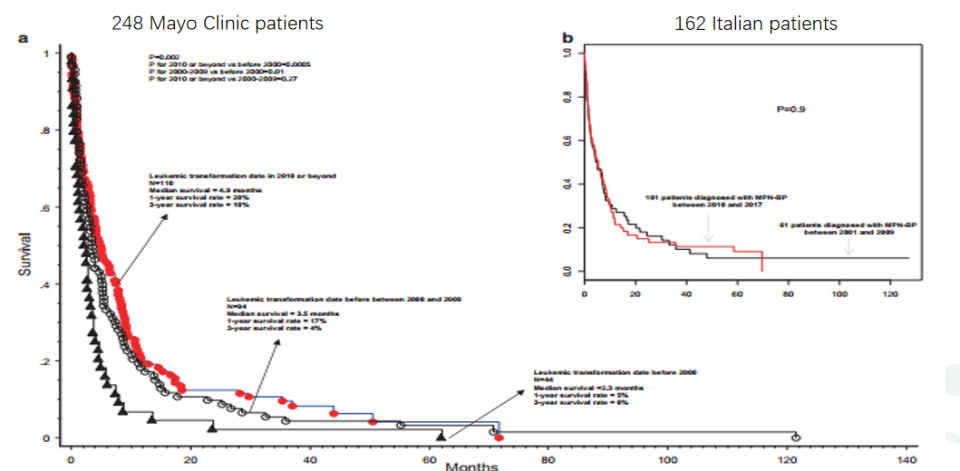
图6.急变期PMF的预后
急变期治疗大致分为两类:一类是芦可替尼联合去甲基化药物,缓解率极低,中位生存时间为6.2~9.5个月;另一类为维奈克拉联合去甲基化药物,缓解率较芦可替尼联合去甲基化药物方案高,但中位生存时间仅为4~7个月。
影响移植预后的因素包括移植技术、KPS及移植前是否完全缓解(CR)。
移植后移植物功能不良(PGF)
17%的患者移植后可能发生PGF,移植后1月时脾脏仍在肋缘下10cm以上是发生移植物功能不良的高危因素之一,其他危险因素还包括输注CD34细胞低、供者特异性抗HLA抗体(DSA)、CMV感染、GVHD、铁超载、骨髓微环境等,但PGF与生存无关。
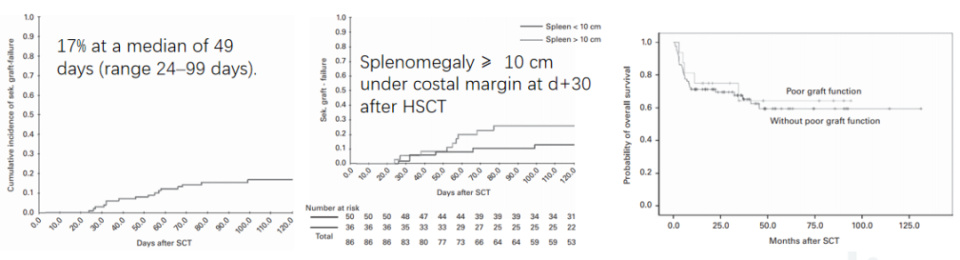
图7. 异基因造血干细胞移植治疗PMF后PGF
陆道培医院数据分享
赵教授分享并总结了近年来陆道培医院开展PMF异基因移植的情况:2015年5月~2023年12月,共17例患者因PMF进行allo-HSCT,其中原发骨髓纤维化15例,继发骨髓纤维化2例,慢性期12例,加速期1例,急变期3例。
单倍体造血干细胞移植(haplo-HCT)10例,相合无关供者(MUD) 6例,HLA配型相合的同胞供者(MSD-HSCT) 1例;
存活患者中位随访时间34个月(3~103个月);
12例慢性期患者5年生存率为82%;
4例死亡病例:2例早期死于感染(1例死于毛霉菌,1例感染性休克),1例继发性移植物功能不良合并感染,1例肝静脉闭塞症(VOD);
专家简介
赵艳丽 教授
陆道培医院骨髓移植科主任(副院长级 )
北京医学会血液分会会员
中国非公医疗血液专委会委员
北京癌症防治移植委员会委员
中国抗癌协会血液病转化医学专业委员会委员
廊坊市医学会血液分会委员
廊坊市抗癌协会常务理事
从事血液及骨髓移植工作20余年,完成异基因骨髓移植1200余例
2011年到美国M.D. Anderson癌症肿瘤中心访问学习
多次参加ASH,EBMT、APBMT做口头及墙报交流