编者按:CAR-T细胞治疗是目前血液领域的研究热点,但如何将CAR-T细胞治疗的临床问题转化为科学研究问题,是困扰广大临床医生的难题。2024年1月26~28日,“中国临床肿瘤学会(CSCO)白血病专家委员会、淋巴瘤专家委员会及骨髓瘤筹备委员会工作会议暨2024年CSCO血液及淋巴瘤、骨髓瘤疾病学术大会”在美丽的海口盛大召开。会上,徐州医科大学血液病研究所所长徐开林教授以《从临床问题到科学问题——CAR-T临床研究的切入点》为题,从5个方面倾情分享了CAR-T细胞治疗从临床问题转化为科学研究问题的经验和体会,对于开展相关方面研究具有重要借鉴和参考意义,本刊特别整理如下。
临床问题1
CAR-T细胞治疗近期疗效让人鼓舞,远期疗效不尽人意,如何提高远期疗效?
首先,CAR-T细胞治疗远期疗效不佳的一个重要原因是,肿瘤干细胞不能被完全杀灭。在多发性骨髓瘤(MM)治疗中,B细胞成熟抗原(BCMA)是一个非常好的靶点,我国已经有相关药物上市,那么如何提高它的远期疗效?大家知道,B细胞受抗原刺激后,分化为浆细胞产生抗体。在这个过程中,CD19抗原虽然丢失很多,在浆细胞上很少有表达,但这个很少表达部分可能代表了骨髓瘤细胞的早期阶段,也就是骨髓瘤样干细胞。面对这样的一个临床问题,如何从临床角度设计能够改善它的远期疗效,我们考虑将抗BCMA和抗CD19的CAR-T细胞组合进行双靶点治疗。研究结果已于2019和2022年分别发表于Lancet Haematol和J Clin Oncol上:
在近期疗效方面:在入组的62例患者中,客观缓解率(ORR)达92%;严格意义的完全缓解/完全缓解(sCR/CR)率达60%以上;微小残留病(MRD)转阴率达77% (43/56)。
在更为关注的远期疗效方面:中位缓解持续时间(DOR)长达20.3个月,提示远期疗效非常不错。此外,中位无进展生存期(PFS)达18.3个月,这也是目前反映CAR-T细胞治疗MM长生存的最好指标,中位总生存期(OS)未达到。在CR及以上患者中,12个月PFS率达89%、OS率达92%。同时,通过比较分析发现,双靶点抗BCMA+CD19 CAR-T细胞治疗的PFS和OS明显优于单靶点抗BCMA CAR-T细胞治疗。
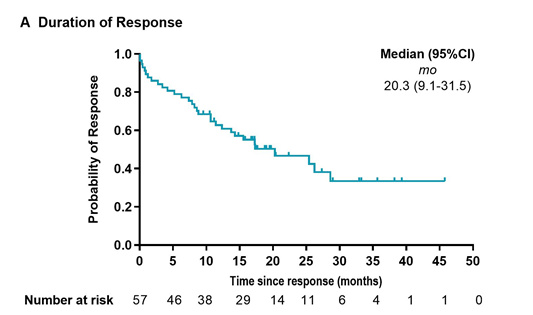
△缓解持续时间(DOR)的Kaplan-Meier分析
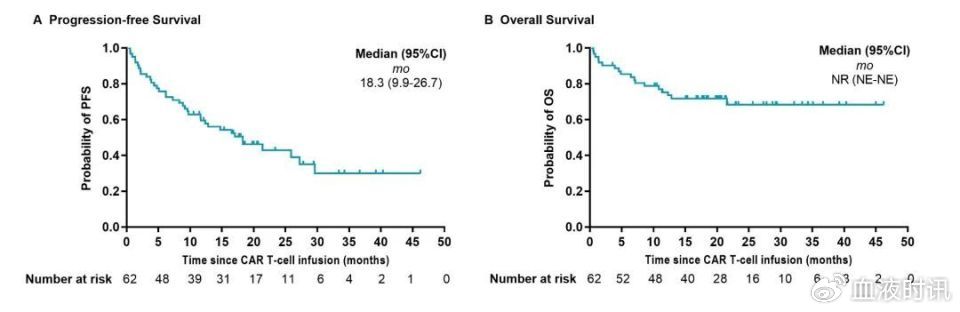
△无进展生存期(PFS)和总生存期(OS)的Kaplan-Meier分析
另一个可提高远期疗效的设计是人源化CAR-T和全人源化CAR-T,徐州医科大学血液病研究所是国内最早推出人源化CAR-T的中心。目前临床上使用的商业化CAR-T依然是以鼠源化CAR-T为主,人对于鼠源化CAR-T的单链抗体可变区具有天然的免疫排斥作用,这可能是导致远期疗效不佳的一个方面。而我们采用人源化CAR-T治疗复发/难治性(R/R)急性B淋巴细胞白血病(B-ALL)的缓解率可以达到90%;在桥接移植后,2年PFS率能够达到80%以上;而且还发现抗药抗体(ADA)阳性与复发相关。
临床问题2
ICANS是CAR-T细胞治疗的主要并发症,CNS B-ALL的疗效及安全性如何?
针对B-ALL合并中枢神经系统(CNS)侵犯,临床缺乏有效治疗手段,治疗效果不理想。CAR-T问世后,我们思考的一个问题是CAR-T细胞是否可以通过中枢,进入中枢后对CNS B-ALL的效果如何?另一个问题是CAR-T细胞治疗有两个相对比较特殊的并发症,分别是细胞因子释放综合征(CRS)、免疫效应细胞相关神经毒性综合征(ICANS),那么ICANS在CNS B-ALL患者中发生率是否更高或更严重?为此,我们牵头将国内几家医院(包括天津市第一中心医院、浙江大学医学院附属第一医院、上海同济大学附属同济医院、华中科技大学同济医学院附属同济医院)记录的资料进行汇总分析,相关工作已发表于2022年Blood上。
研究共入组48例患者。结果显示:在骨髓中ORR达88%,在中枢中缓解率也达到了85%,二者差别不大;桥接治疗组疗效更优;中位OS达16.0个月,中位无事件生存期(EFS)达8.7个月,这提示CAR-T细胞治疗可以通过血脑屏障进入中枢,而且可以起到不错的治疗作用。另外,在中枢神经毒性方面,脑病的发生率为22.9%,其中≥3级的发生率为8.3%,因此中枢神经毒性的发生率没有想象中那么高,处理起来也没有那么可怕。相信未来随着CAR-T结构的优化、不良事件的进一步减少,尤其是价格的降低,CAR-T细胞治疗将在CNS B-ALL中发挥巨大潜力。
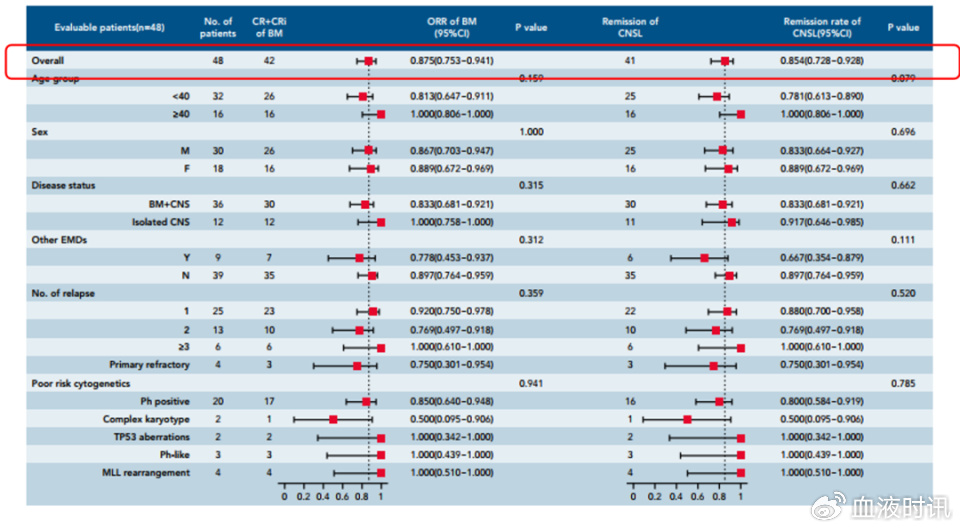
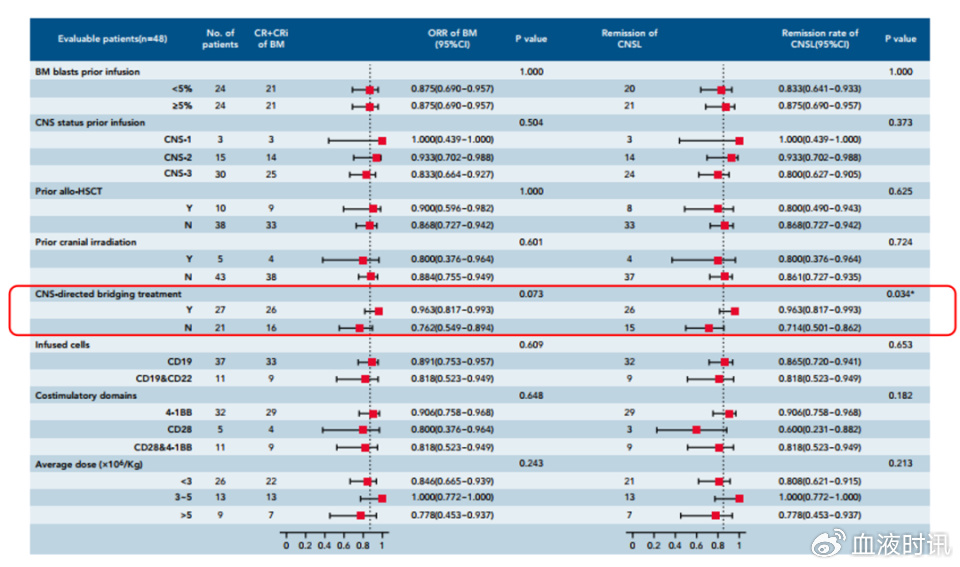
△缓解率和亚组分析
临床问题3
中国是一个人口大国,HBV相关感染需高度重视,CAR-T细胞治疗对HBV再激活及肝功能的影响?
针对免疫治疗可能带来的不良事件,我国是乙肝病毒(HBV)相关感染大国,那么CAR-T细胞治疗后是否会对HBV或肝功能产生影响?大家知道,CD20单抗用于弥漫大B细胞淋巴瘤治疗时,非常少的患者会发生HBV的再激活,而CAR-T的免疫治疗强度较CD20单抗更大,那么是否会带来这方面问题?我们总结了70例患者,其中12例伴有慢性HBV感染,29例既往有HBV感染,29例无任何HBV感染证据。该研究结果已于2020年发表于Leukemia上。结果显示,2/12慢性HBV感染患者及1/29既往HBV感染的血液肿瘤患者出现HBV再激活,而29例无任何HBV感染患者未出现新HBV感染。这提示对于慢性HBV感染的患者CAR-T治疗前开始预防性抗HBV治疗是非常必要的;对于既往有感染的患者也应密切观察,一旦发生HBV再激活,同样应进行抗HBV治疗。此外,研究还发现,慢性或既往HBV感染并不影响CAR-T细胞治疗的疗效,也不增加CRS及神经毒性的发生率及严重程度。
临床问题4
CAR-T细胞治疗多发性骨髓瘤(MM)缓解后再复发或进展的患者,如何选择下一步治疗?
CAR-T细胞治疗后复发怎么办?这是大家经常会提到的问题。以多发性骨髓瘤(MM)为例,我们开展了抗 GPRC5D CAR-T治疗R/R MM的Ⅱ期临床试验,目前研究结果已发表于J Clin Oncol上。共有33例患者入组,ORR达到91%,与目前已上市的抗BCMA CAR-T疗效相似;sCR/CR率也达到63%,因此GPRC5D是继BCMA后非常有竞争力的一个靶点。其中我们更为关注的是BCMA治疗失败或治疗进展的9例患者,其中包括2例反复接受过抗BCMA CAR-T细胞输注但最后一次没有反应的患者,这2例患者在接受抗 GPRC5D CAR-T治疗后分别获得CR和部分缓解(PR),其余7例患者均为抗BCMA CAR-T细胞治疗后疾病复发或进展的患者。总体而言,9例患者在接受抗GPRC5D CAR-T细胞治疗后,4例达到CR,2例达到非常好的PR(VGPR),3例达到PR。
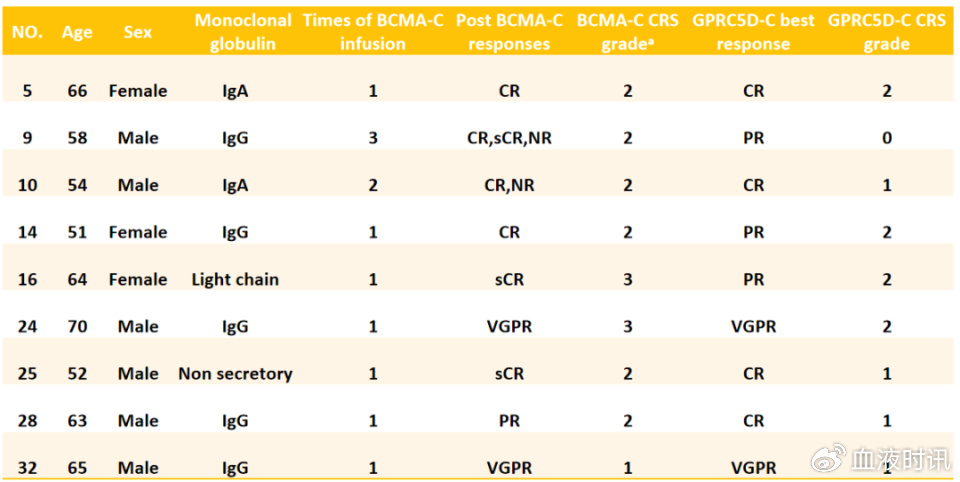
抗GPRC5D CAR-T细胞在既往接受抗BCMA CAR-T细胞治疗患者中的反应和毒性
安全性方面,在观察的33例患者中,CRS发生率为76%,无3级CRS;神经毒性发生率也较低,其中ICANS 2级和3级各1例,头痛3级1例。但是也有一些特殊的并发症,主要由脱靶造成的,没有给患者造成明显不适,如指甲脱落造成的指甲炎,发生率达30%,但患者的老指甲脱掉后,新指甲又会长出来,所以影响不大。针对抗BCMA CAR-T治疗后复发患者,换成新的靶点CAR-T,让患者又多了一个选择。前面提到我们中心抗BCMA CAR-T最好的疗效可以使患者中位PFS达到18.3个月,如果复发患者再接受新靶点CAR-T治疗,则可使患者得到更多长生存的机会。
临床问题5
CAR-T作为过继免疫细胞治疗,而最常用靶点BCMA和CD19分别作用于浆细胞和B细胞,对体液免疫重建有何影响?
BCMA、GPRC5D作用于浆细胞,或CD19作用于B细胞,均给体液免疫造成影响,那么这些影响是否会给患者带来严重后果?我们观察了抗BCMA CAR-T治疗后外周血B细胞和骨髓浆细胞的动态变化。结果发现,所有患者均出现B细胞再生障碍(BCA)。B细胞计数在CAR-T输注后中位7天降至最低;CAR-T细胞输注后的2个月,B细胞计数处于持续低下状态。中位97天恢复基线水平,中位177天恢复正常。正常浆细胞在中位212天第一次被检测到。然而,这种对体液免疫的影响并不严重而且是可以处理的,临床上可以静脉补充免疫球蛋白,让患者安全度过免疫抑制期。
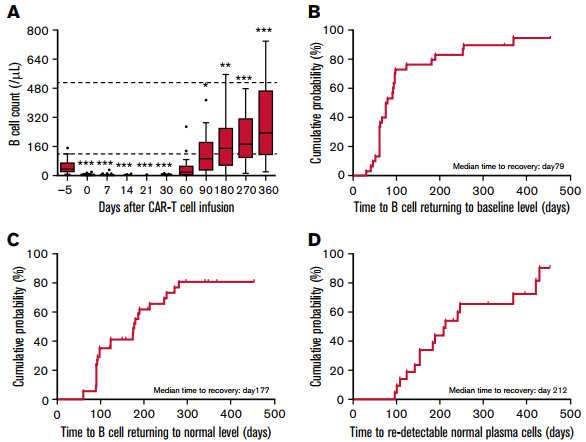
△抗BCMA CAR-T细胞治疗患者B细胞恢复的动力学
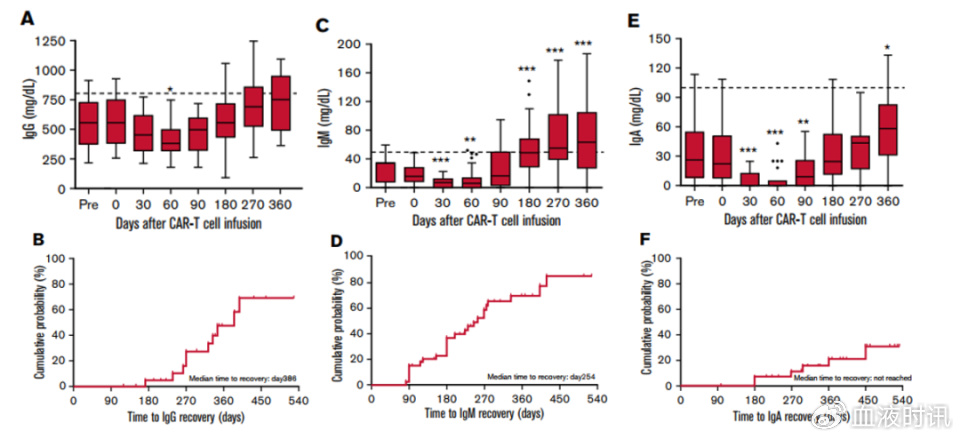
△抗BCMA CAR-T细胞治疗患者血清IgG、IgM和IgA恢复的动力学
参考文献:
[1]Yan Z, Cao J, Cheng H, et al. A combination of humanised anti-CD19 and anti-BCMA CAR T cells in patients with relapsed or refractory multiple myeloma: a single-arm, phase 2 trial. Lancet Haematol. 2019 Oct;6(10):e521-e529. doi: 10.1016/S2352-3026(19)30115-2. Epub 2019 Aug 1. PMID: 31378662.
[2]Wang Y, Cao J, Gu W, et al. Long-Term Follow-Up of Combination of B-Cell Maturation Antigen and CD19 Chimeric Antigen Receptor T Cells in Multiple Myeloma. J Clin Oncol. 2022 Jul 10;40(20):2246-2256. doi: 10.1200/JCO.21.01676. Epub 2022 Mar 25. PMID: 35333600.
[3]Cao J, Wang G, Cheng H, et al. Potent anti-leukemia activities of humanized CD19-targeted Chimeric antigen receptor T (CAR-T) cells in patients with relapsed/refractory acute lymphoblastic leukemia. Am J Hematol. 2018 Jul;93(7):851-858. doi: 10.1002/ajh.25108. Epub 2018 Apr 28. PMID: 29633386.
[4]Shi M, Li L, Wang S, et al. Safety and efficacy of a humanized CD19 chimeric antigen receptor T cells for relapsed/refractory acute lymphoblastic leukemia. Am J Hematol. 2022 Jun 1;97(6):711-718. doi: 10.1002/ajh.26506. Epub 2022 Feb 25. PMID: 35179242.
[5]Qi Y, Zhao M, Hu Y, et al. Efficacy and safety of CD19-specific CAR T cell-based therapy in B-cell acute lymphoblastic leukemia patients with CNSL. Blood. 2022 Jun 9;139(23):3376-3386. doi: 10.1182/blood.2021013733. PMID: 35338773.
[6]Wang Y, Liu Y, Tan X, et al. Safety and efficacy of chimeric antigen receptor (CAR)-T-cell therapy in persons with advanced B-cell cancers and hepatitis B virus-infection. Leukemia. 2020 Oct;34(10):2704-2707. doi: 10.1038/s41375-020-0936-4. Epub 2020 Jun 27. PMID: 32594100.
[7]Xia J, Li H, Yan Z, et al. Anti-G Protein-Coupled Receptor, Class C Group 5 Member D Chimeric Antigen Receptor T Cells in Patients With Relapsed or Refractory Multiple Myeloma: A Single-Arm, Phase Ⅱ Trial. J Clin Oncol. 2023 May 10;41(14):2583-2593. doi: 10.1200/JCO.22.01824. Epub 2023 Mar 7. PMID: 36881785; PMCID: PMC10414745.
[8]Wang Y, Li C, Xia J, et al. Humoral immune reconstitution after anti-BCMA CAR T-cell therapy in relapsed/refractory multiple myeloma. Blood Adv. 2021 Dec 14;5(23):5290-5299. doi: 10.1182/bloodadvances.2021004603. PMID: 34587230; PMCID: PMC9153033.
专家简介
徐开林 教授
徐州医科大学血液病研究所所长
博士、二级教授、博士生导师
江苏省骨髓干细胞研究所所长
徐州医科大学造血干细胞移植中心主任
中华医学会血液学分会第九、十届委员会委员、实验诊断学组副组长
中国医师协会血液科医师分会常委
江苏省血液学分会前任主任委员
江苏省医师协会血液科医师分会会长
国家自然科学基金初审、终审专家
卫生部及江苏省有突出贡献的中青年专家
享受国务院政府特殊津贴
作为课题负责人承担科研课题20余项,其中主持国家自然科学基金重点项目1项,CAR-T细胞治疗专项1项,面上项目8项,省部级课题10余项,发表论文180余篇,其中包括JCO,Blood,Lancet haematology, Leukemia,Haematologica,Am J Hematol等杂志发表SCI收录论文90篇。以第一获奖者先后获得科技成果奖16项,其中教育部高等学校科学研究优秀成果奖(科学技术)二等奖2项,中华医学科技奖三等奖1项,省科技进步二等奖1项