编者按:2024年4月14日至17日,第50届欧洲血液和骨髓移植学会(EBMT)年会在英国格拉斯哥隆重举行。会议聚焦干细胞移植和细胞疗法的最新进展,推动血液病及血液肿瘤患者向着更好的临床预后迈进。本期特邀杨林花教授分享精选的异基因造血干细胞移植领域和细胞免疫治疗领域进展,欢迎各位读者交流分享。

文献1
PTCy时代非亲缘HLA错配HCT患者生存分析:EBMT细胞治疗和免疫生物学工作组的一项综合研究。
主要作者:Esteban Arrieta Bolaños(德国)
研究背景
HLA匹配是目前异基因造血干细胞移植的主流,目前移植更倾向于选择相合的非亲缘供者(UD)。目前移植后环磷酰胺(PTCy)用于GVHD的预防,提高了非亲缘HLA错配HCT可及率,但具体作用仍不清楚。
研究方法
该研究分析了2016-2020年间EBMT登记的17276例成人血液恶性肿瘤患者中接受非亲缘相合造血干细胞移植(UD-HCT)结果。AML、ALL、MDS及MPN为主,占67.5%,其中66.2%患者接受HCT,减低预处理强度(RIC) 56%,非体外去T 76%。23.5%为1个(9/10;N=3 561)或2个(8/10;n=499)高分辨率HLA错配(mM)。7%(n=924)的10/10患者和15% (n=599)的<10/10患者使用了PTCy,其他所有患者接受了标准的钙调磷酸酶抑制剂预防GvHD。通过构建多因素模型分析了使用或不使用PTCy时HLA mM的数量、种类、位点、分辨率(等位基因vs抗原)和功能[抗原识别域(ARD)、肽结合基序(PBM)]对HCT结局影响。
研究结果
随访60个月时,HLA mM移植的OS更差(8/10为45%,9/10为47%,10/10为52%;P<0.001;图1a)。
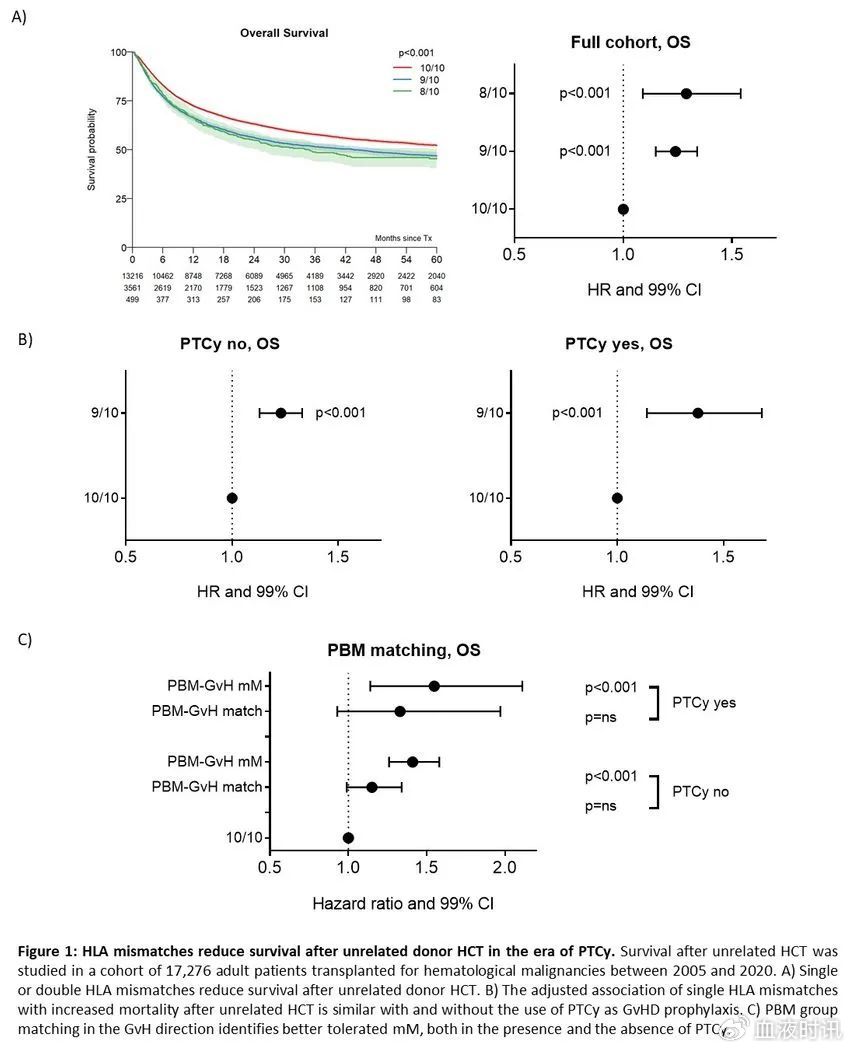
多因素分析显示,1个(HR 1.24 [99% CI 1.15-1.34];P<0.001)或2个 (HR 1.29 [1.09-1.54];P<0.001)位点错配与10/10移植相比,均与更高的死亡风险相关。即便排除ARD错配,HLA I类抗原错配也与明显较差的OS相关(HR 1.31 [1.20-1.42];P<0.001),其中HLA-A(HR 1.37 [1.21-1.54];P<0.001)和HLA-B(HR 1.44 [1.23-1.69];P<0.001)比HLA-C mM(HR 1.16 [1.01-1.33];P=0.005)具有更高的风险,抗原水平比等位基因mM与更差的OS相关(HR 1.22 [1.01-1.46];P=0.006)。而HLA II类错配对OS无统计学差异(HR 1.07 [0.93-1.22];P=0.23);在GRFS、RFS、NRM和aGVHD中也观察到类似的结果,但在复发或慢性GvHD中没有显著差异。
不容许的HLA-DPB1 mM增加了9/10和10/10移植中aGvHD的风险。与标准预防相比,PTCy的使用显著降低了GvHD的风险和死亡率,但并没有改善HLA mM的不良影响。在使用PTCy(HR 1.38 [1.14-1.68];P<0.001)和不使用PTCy的情况下(HR 1.23 [1.13-1.33];P<0.001),单个mM都会显著增加死亡风险(图 1b)。

与GvH-PBM错配相比,无论是否使用PTCy预防GVHD,GvH-PBM匹配的患者OS均更优(HR 1.2 [1.02-1.4];P=0.004)(图1c)。

研究结论
目前HCT中,非亲缘HLA不相合与死亡风险增加相关,主要由HLA I类抗原错配驱动。即使使用PTCy预防GvHD,也无法改善这一风险,选择更佳的错配供者(例如PBM匹配)有望改善HCT结局。
文献2
一项II期前瞻性研究的最终分析:在清淋时疾病进展的DLBCL患者CAR-T扩增时加入纳武利尤单抗
主要作者:Odelia Amit (以色列)
研究背景
背景:清淋(lymphodepletion,LD)时快速病情进展(PD)的患者获得CR的比例较低,6个月的PFS仅20-30%。过去的研究证明,改进CAR-T细胞的体内扩增可以克服这种严重的不良影响并改善预后[Bone Marrow Transplant 57 (Suppl 1), 11–15 (2022)]。本次报道在CAR-T治疗中加入纳武利尤单抗的最终分析结果。本研究的目的是通过“开启”免疫系统和诱导更大的CAR-T细胞扩增来改善临床反应。结果显示纳武利尤单抗可通过安全有效的体内扩增CAR-T细胞提高早期治疗缓解率,如何持久发挥作用,需进一步研究。
研究方法
这项前瞻性II期研究(NCT05385263)纳入在清淋之前PD的DLBCL患者。在CAR-T输注后5-9天,入组患者接受纳武利尤单抗(3 mg/kg)。+7天<100 CAR-T细胞/ul的患者在第19天给予额外剂量的纳武利尤单抗。终点包括安全性、疾病缓解评估和缓解持续时间。
研究结果
入组20例患者,接受抗CD19 CAR-T治疗(Axicabtagene ciloleucel, n=12;Tisagenlecleucel,n=8)。中位年龄67岁(范围40-77岁),6例(30%)患者ECOG评分1。淋巴细胞清除(LD)前中位LDH为528(范围367-1279)U/L。
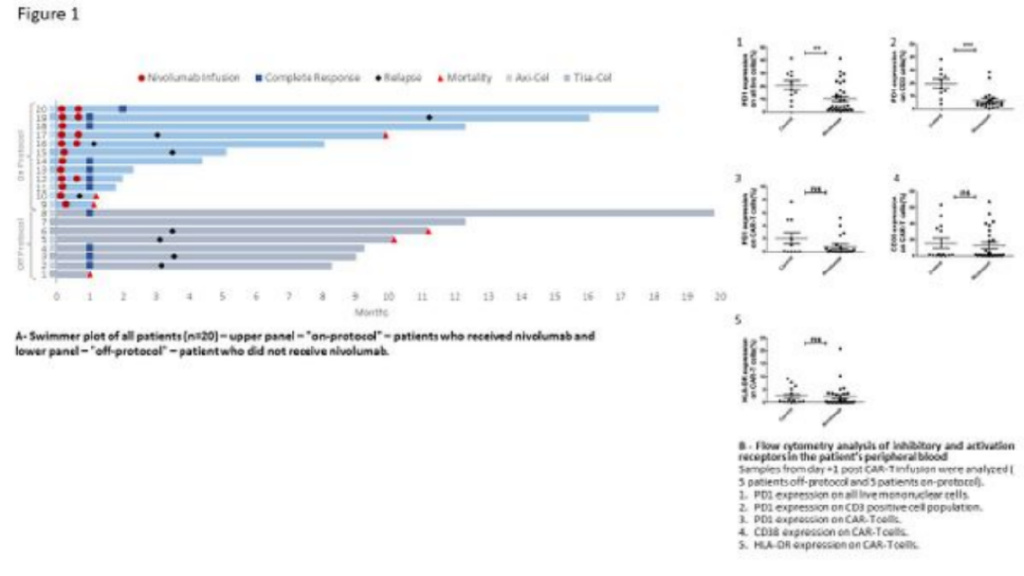
因活动性CRS(n=6)和/或ICANS(n=3),8例(40%)患者不适合纳武利尤单抗治疗(非方案组),12例患者进入纳武利尤单抗组(方案组,7例仅接受1剂,图1a)。
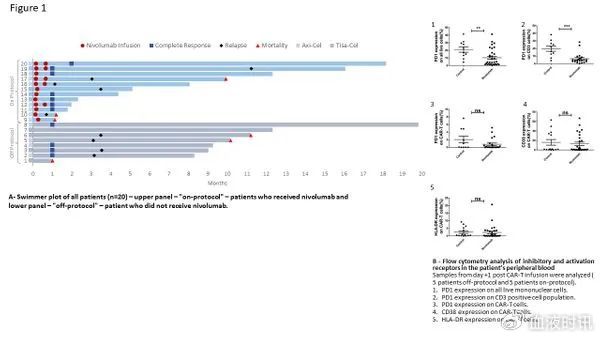
8例与纳武利尤单抗相关的AE,其中发热4例、皮疹2例、腹泻1例、中性粒细胞减少1例,未观察到与之相关的SAE。1例患者死于迟发性延长的全血细胞减少和复发性败血症。
10例患者流式细胞术检测显示,67%的患者出现CAR-T细胞再扩增,与对照组相比,方案组患者在单个核细胞和CD3+T细胞上的PD-1表达均显著降低[分别为10.2% vs. 21%(P=0.0075)和6.5% vs. 19.7%(P=0.0009)],而在CAR-T细胞上的PD-1表达(P=0.52)、活化标记物及T细胞亚群,两组之间无差异。
所有患者中,ORR为80%(CR,n=12,60%;PR,n=4,20%)和PD (n=3, 15%),1例患者无复发死亡,疗效未进行评估。优于历史对照(CR, n=16,39%,PR,n=10,24%,PD,n=15,37%)。6个月时,48%的患者无进展,85%的患者存活。与基线问卷相比,3个月EORTC QLQ-C30问卷显示整体健康感知(P=0.025)和整体生活质量(P=0.059)有所改善,方案组和非方案组之间无差异。
研究结论
根据CAR-T扩增调整的纳武利尤单抗对于LD时PD的患者是安全的,且与优秀的缓解率相关。但缓解持续时间仍不足,未来的研究需要解决这个问题才能进一步改善生存。
文献3
年轻移植后复发ALL的有效治疗:Tisagenlecleucel批准后的真实世界研究
作者:Laura M. Moser(德国)
研究背景
由于治疗方案十分匮乏,高危ALL在HSCT后复发是一项重大挑战。Tisagenlecleucel(Tisa-cel)是一种靶向CD19的CAR-T细胞疗法,既往研究在移植后复发的≤25岁患者中取得了令人鼓舞的疗效。
研究方法
研究纳入了2018年9月至2023年9月期间来自28个欧洲中心210例接受Tisa-cel治疗的移植后复发的患者,评估其疗效。患者中位年龄10岁(0.9-25.3岁)。
研究结果
HSCT预处理方案包括:93例患者(55%)接受TBI;39例(23%)接受以苏消安为基础的方案;35例(21%)接受以白消安为基础(其他1例,不明确42例)。HSCT后早期复发(移植后6个月内)55例(26%),晚期复发患者(移植6个月后)154例(74%)。在清淋(LDC)之前,62%的患者骨髓白血病细胞<5%(23% MRD-;39% MRD+),38%患者骨髓白血病细胞≥5%。在CAR-T治疗后第28天,196例患者(93%)达到完全缓解(CR),2例患者(1%)死于CAR-T细胞相关毒性。124例(59%)患者出现细胞因子释放综合征(CRS),其中16例(8%)患者CRS分级≥3级。免疫效应细胞相关神经毒性综合征(ICANS)发生25例(12%),ICANS分级≥3级10例(5%)。
中位随访30.0个月(范围0.6-59.9),2年EFS为42.1%(±3.9%),2年OS为66.5%(±3.7%)。非复发死亡率为1.1%(±0.7%)。LDC前的白血病负担和HSCT后复发的时间显著影响预后,LDC时MRD-患者的2年EFS(56.8%±8.7%)和2年OS(80.7%±6.8%)显著高于MRD+患者(EFS 48.1%±6.1%;OS 68.8%±5.8%)或非缓解期(NR)患者(EFS 27.3%±5.8%;OS 54.4%±6.3%)。早期复发患者的EFS(21.5%±7.2%)和OS(45.9%±7.8%)均低于晚期复发患者(2年EFS 48.7%±4.6%;OS 73.6%±4.0%,P<0.001)。晚期复发患者的累积复发率(CIR)较低(47.4%±4.6% vs. 68.1%±8.2%,P=0.019)。
CAR-T输注2年后,持续B细胞发育不全的比例为37.3%(±4.5%)。CAR-T输注2年后复发以CD19+居多(2-yr CIR 33.3% ±3.8% vs. 15.5% ±2.7%),CD19-复发发生更早,预后更差:CD19+复发的2年OS为39.9%(±7.4%),而CD19-复发的2年OS为23.3%(±8.3%)(P=0.007)。
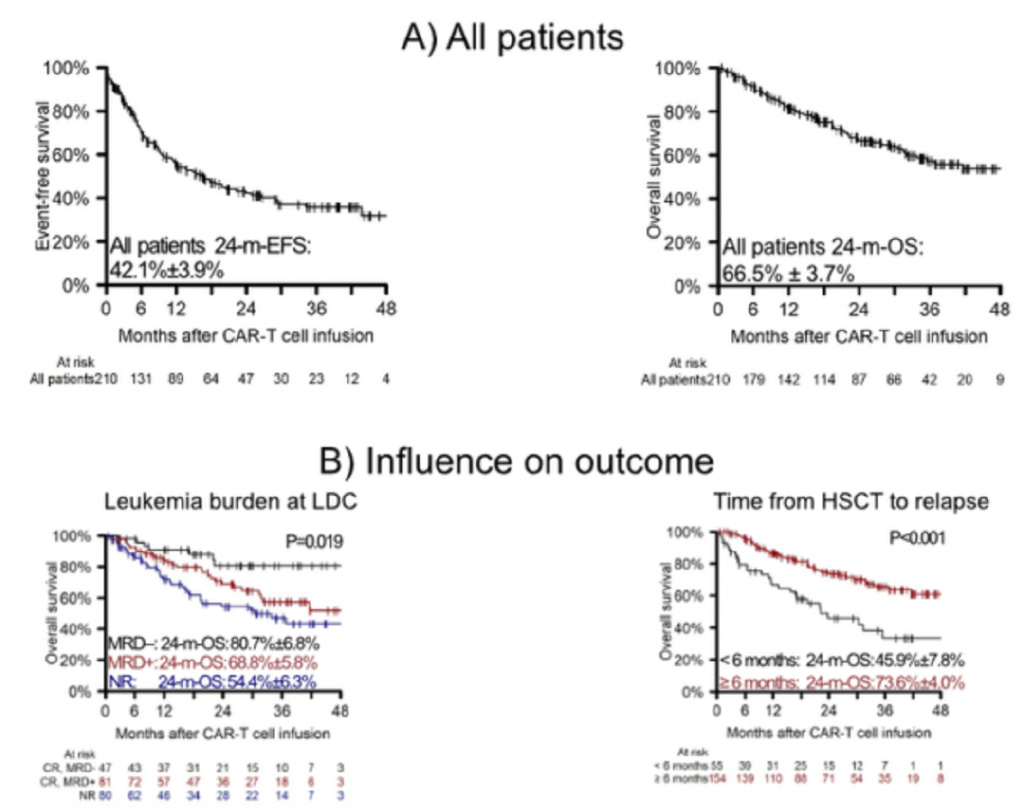
研究结论
欧洲的真实数据表明,在HSCT后≥6个月复发的儿童和年轻成人患者中,Tisa-cell治疗是有前景的。值得注意的是,清淋时的白血病负担和HSCT后早期复发被认为是EFS和OS的不利因素。研究结果强调需要针对这些高危人群制定更有效的替代治疗策略。

专家简介
杨林花
二级教授 博士生导师 国务院特殊津贴专家
山西医科大学第二医院血液科 山西医科大学血液病研究所所长
中华医学会血液学会常委
中国医药教育协会血液专业委员会副主任委员
中国研究型医院协会血液病精准诊疗专业委员会副主任委员
中国老年医学学会理事
CSCO中国白血病淋巴瘤常委
中国女医师协会血液肿瘤专业委员会常委
中国病理生理学会血液免疫分会常委
山西省医师协会血液医师分会会长
山西省抗癌协会白血病淋巴瘤专业委员会主任委员
山西省新兴产业领军人才
山西省三晋英才高端领军人才
《Hemophilia》、《Blood》中文版编委、《中华血液学杂志》、《中华内科杂志》、《中华全科医师杂志》等杂志编委