编者按:2024中国临床肿瘤学会(CSCO)指南会如约而至,多部CSCO肿瘤诊疗指南一如既往地迎来更新或首次发布。在血液肿瘤领域,备受关注的CAR-T细胞治疗指南进行了重要更新,由《CSCO CAR-T细胞治疗恶性血液病及免疫靶向治疗相关感染管理指南2023》(简称2023版指南)更名为《CSCO CAR-T细胞治疗恶性血液病指南2024》(简称2024版指南)。会上,同济大学附属同济医院、同济大学血液病研究所张文君教授对2024版指南的更新要点进行了精彩分享,本刊特整理如下,以飨读者。
2024版指南共包括四个章节:第一,靶向CD19 CAR-T细胞治疗B细胞非霍奇金淋巴瘤(B-NHL);第二,靶向BCMA CAR-T细胞治疗多发性骨髓瘤(MM);第三,靶向CD19 CAR-T 细胞治疗成人复发/难治性急性B淋巴细胞白血病(R/R B-ALL);第四,CAR-T 治疗不良反应管理。与2023版指南相比,最大的不同是新增了第四章节“CAR-T治疗不良反应管理”,此外在其余3个章节也有重要更新。
CAR-T治疗不良反应管理
01.细胞因子释放综合征(CRS)
2024版指南根据美国移植和细胞治疗学会(ASTCT)分级系统,综合发热、低血压、低氧血症三个临床表现将CRS的严重程度由低到高分为4个级别。
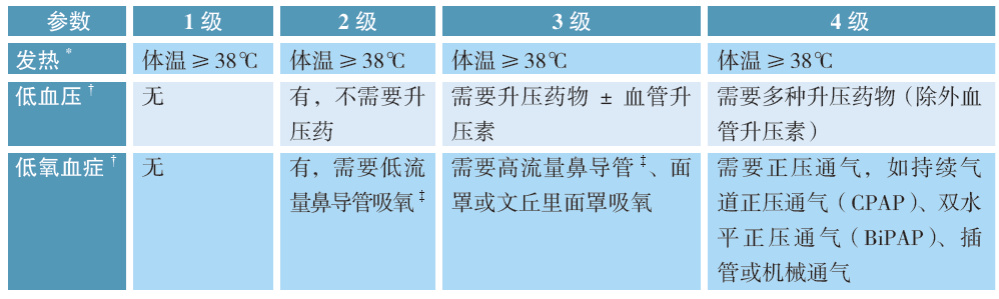
根据不同分级选择相应处理方法。其中托珠单抗单次治疗最大剂量为800 mg,可重复给药;治疗后24小时CRS无改善甚至加重,应升级至下一级处置措施;托珠单抗和类固醇的早期干预不会影响B-ALL、B-NHL中CD19 CAR-T细胞的扩增和疗效。
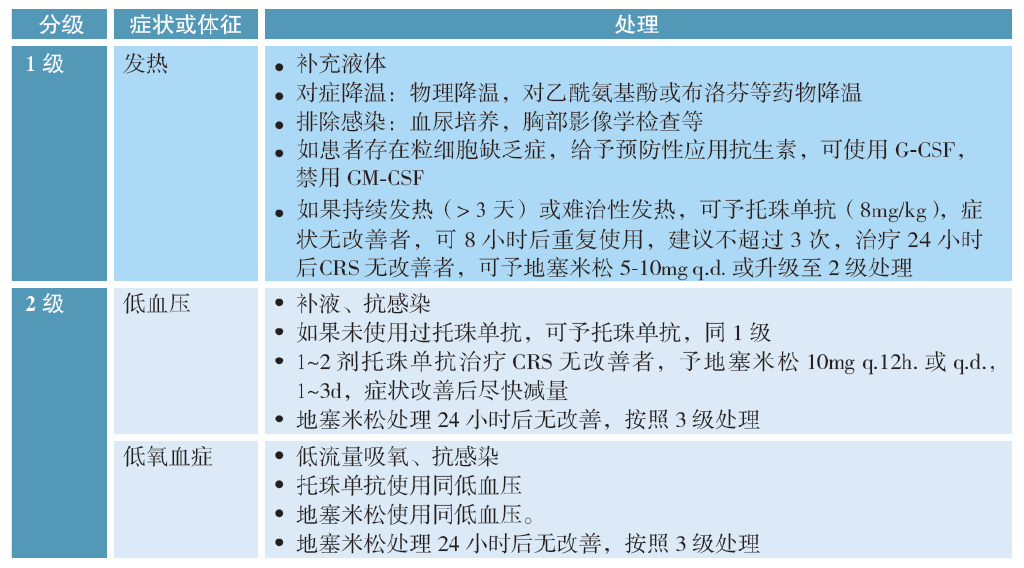

需要指出的是,新版指南尚未推荐司妥昔单抗、芦可替尼、达沙替尼用于CRS的治疗,以及血浆置换用于严重CRS的治疗。
02.免疫效应细胞相关神经毒性综合征(ICANS)
2017年Neelapu团队首先提出“CAR-T细胞相关性脑病综合征(CRES)”的概念,2019年美国移植和细胞治疗学会(ASTCT)进一步提出了“免疫效应细胞相关神经毒性综合征(ICANS)”的概念。ICANS 的定义较CRES更为准确地反映了神经系统病变的病理生理学特征,在目前临床诊断和治疗中获得了更广泛的认可和应用。本指南使用ICANS 命名CAR-T细胞治疗相关神经系统毒副反应。根据CAR-T细胞疗法相关的毒性(CARTOX)10分法(CARTOX-10)和免疫效应细胞相关脑病(ICE)评分建立ICANS分级系统。
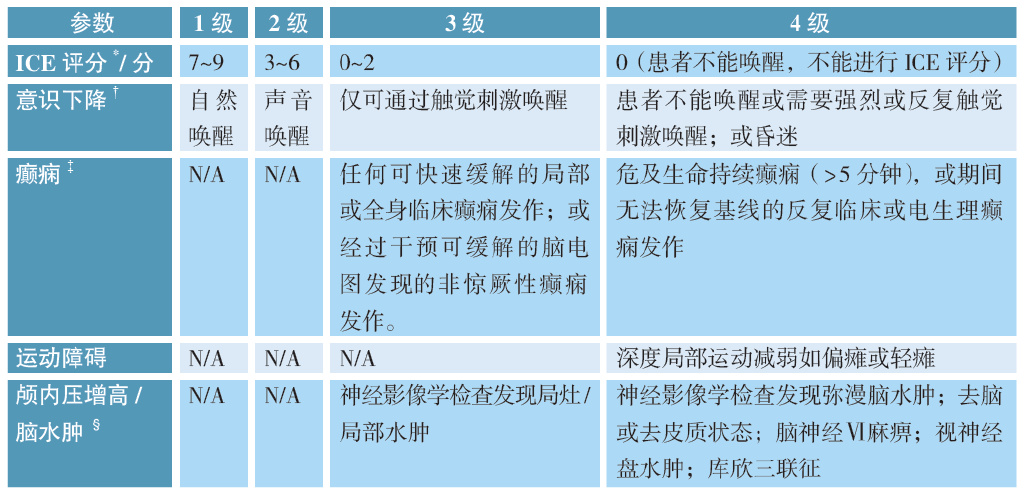
根据不同分级选择相应处理方法。其中由于托珠单抗与白介素6(IL-6)受体结合导致血清游离IL-6水平升高,进一步增加脑脊液中IL-6浓度,有可能加重神经毒性。因此,在ICANS 的处理过程中,糖皮质激素的使用较托珠单抗更重要。

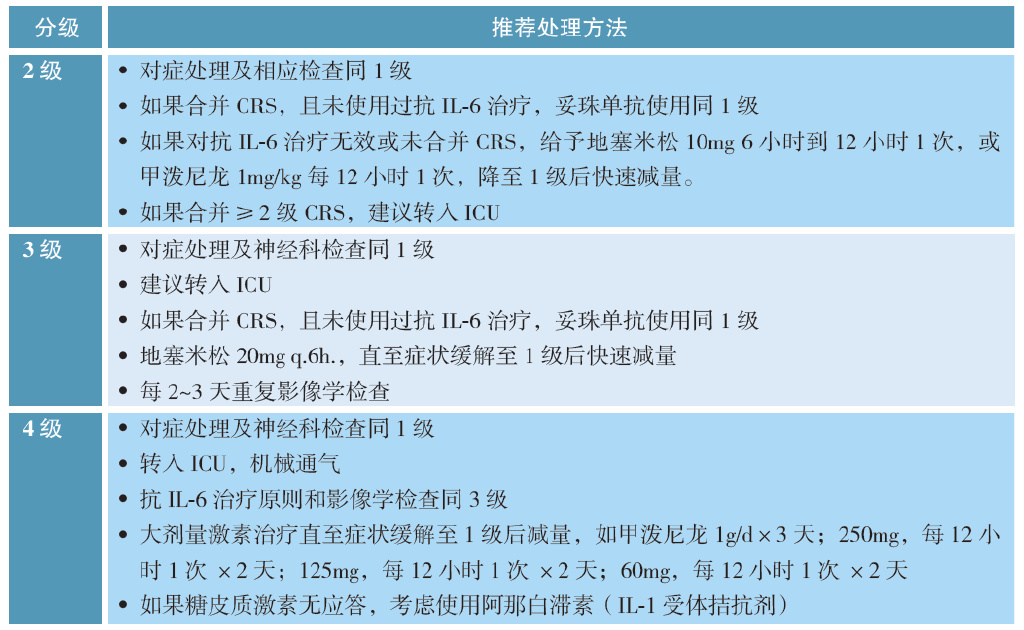
此外,针对特殊群体的毒性反应管理包括:(1)ALL:CRS 和ICANS是管理重点。高肿瘤负荷免疫毒性更强,处理需更积极。ALL高肿瘤负荷(骨髓原始细胞≥40%)的患者,若高温持续不退,可直接使用托珠单抗治疗;低肿瘤负荷患者按标准疗法。(2)NHL:多学科协作(MDT)全流程管理、局部CRS、各环节CRS、ICANS风险识别和干预参考《CAR-T细胞治疗NHL毒副作用临床管理专家共识》。(3)MM:与靶点相关独特的不同迟发性神经毒性。迟发性神经毒性包括颅神经麻痹(最常见的为第7颅神经麻痹)、神经病变和帕金森样综合征。迟发性神经毒性背后的机制尚不清楚,但中枢神经系统中低水平的BCMA表达和介导靶向脱靶效应的CAR-T细胞的迁移可能起作用。
03.免疫效应细胞相关噬血细胞性淋巴组织细胞增生症样综合征(IEC-HS)
IEC-HS是一种独立于CRS和ICANS的病理和生化过度炎症反应综合征。其特点有:(1)表现为巨噬细胞活化(MAS)/噬血细胞淋巴组织细胞增生(HLH)的特征;(2)归因于免疫效应细胞治疗,被认为是CRS 处理过程后的延迟表现;(3)加重或新发的血细胞减少症、高铁蛋白血症、伴有低纤维蛋白原血症的凝血异常和/或转氨酶异常。IEC-HS可根据常见的临床或实验室表现(如铁蛋白升高、CRS治疗初步改善或CRS消退后出现炎症反应加重、肝转氨酶升高等)和其他临床或实验室表现(如乳酸脱氢酶升高、其他凝血异常、高直接胆红素血症等)进行诊断,并根据症状严重程度采取相应干预措施。

由于缺乏前瞻性研究和IEC-HS治疗方法的数据,因此治疗建议来自于专家意见、CRS/IEC-HS队列的证据和/或先前对原发性噬血细胞性淋巴组织细胞增生症(pHLH)和继发性噬血细胞性淋巴组织细胞增生症(sHLH)的治疗分析。目前对于三线及后续治疗方案的选择较多,建议根据患者的具体情况采用相应的治疗方法。

此外,针对IEC-HS还可以从监测、血细胞减少症、凝血功能障碍、感染四个方面进行支持治疗,如每日监测血常规、凝血功能和纤维蛋白原;维持血红蛋白>7 g/dL;使用冷沉淀物或替代纤维蛋白原进行积极治疗,维持纤维蛋白原水平>100 mg/dL(不伴出血)和> 150 mg/dL(伴出血);经验性抗感染管理等。
04.CAR-T相关出凝血性疾病(CARAC)
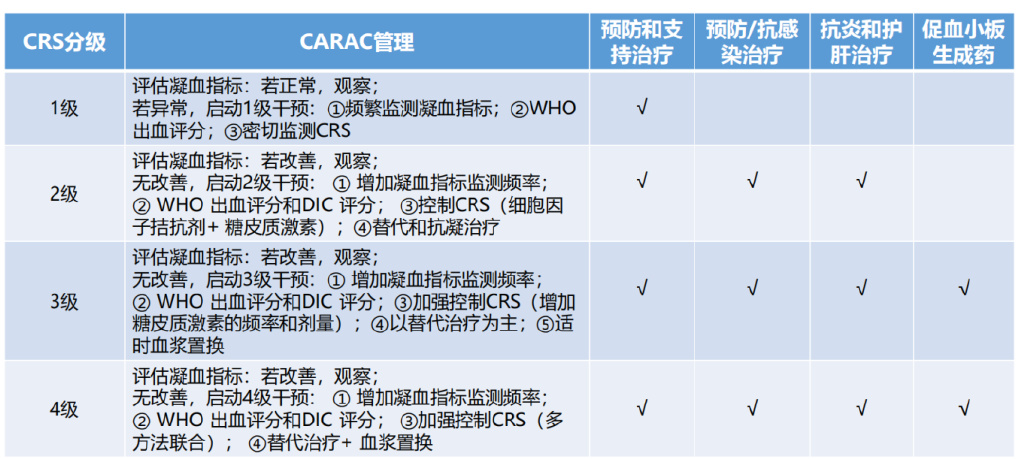
CARAC是指CAR-T细胞回输后近期内,与细胞因子释放相关,以出血和/或血栓为特征,伴随血小板下降及凝血指标异常的临床综合征。临床表现有:患者常有血栓及弥散性血管内凝血(DIC)等并发症,表现为肺栓塞、深静脉血栓、皮肤瘀点/瘀斑、黄疸、低血压、呼吸困难等,实验室检查结果显示血小板下降及凝血指标异常。根据不同CRS分级,进行相应CARAC管理,推荐的处理方法包括预防和支持治疗、预防/抗感染治疗、抗炎和护肝治疗、促血小板生成药。
05.免疫效应细胞相关血液毒性(ICAHT)
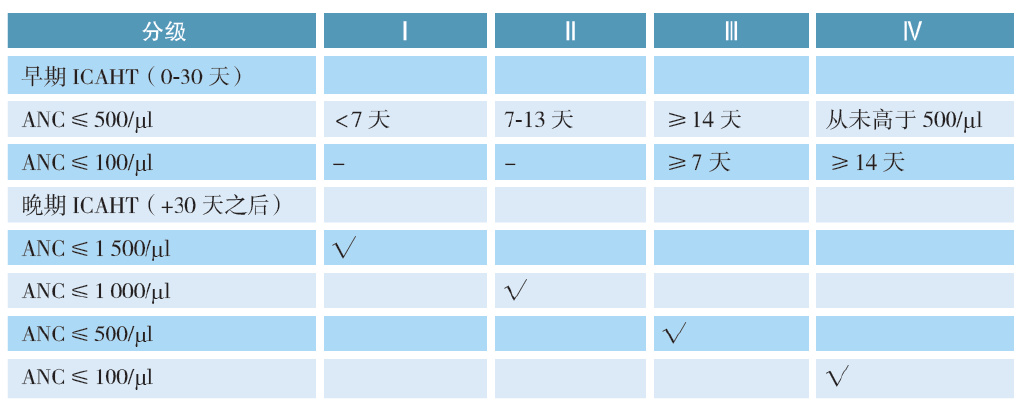
2023年Blood发布了《免疫效应细胞相关血液毒性(ICAHT):EHA/EBMT共识分级和最佳实践建议》。根据该建议将ICAHT分为早期ICAHT和晚期CAHT,并结合中性粒细胞计数(ANC)水平,将ICAHT的严重程度分为4个等级。
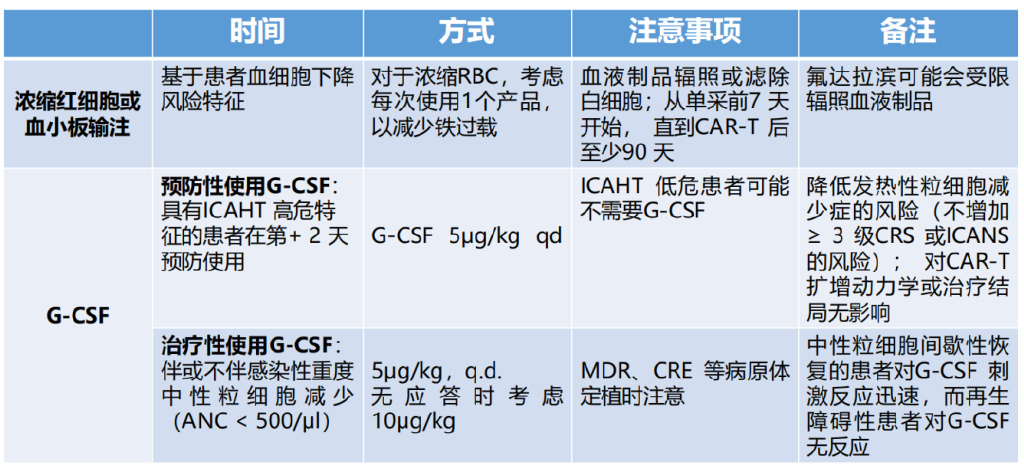
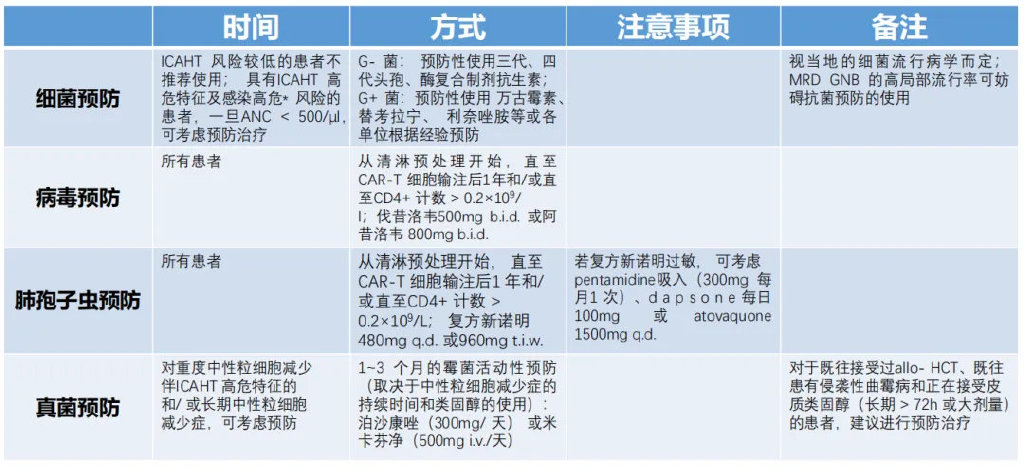
针对ICAHT的短期管理,推荐的处理方法有:浓缩红细胞或血小板输注、预防性或治疗性使用粒细胞集落刺激因子(G-CSF)以及针对特定患者的细菌/真菌预防、针对所有患者的病毒/肺孢子虫预防。
06.B细胞缺乏症/ 低丙种球蛋白血症
B细胞发育不全被定义为一种由B细胞耗竭或缺失引起的疾病。CAR-T诱导的B细胞发育不全的机制为靶向CD19的CAR-T的细胞疗法靶外肿瘤效应(on-target off-tumor effect),可降低B细胞计数和丙种免疫球蛋白的水平。研究显示,CAR-T 回输后不同时间段均可能发生低丙种球蛋白血症,90天后发生率约67%,少数患者甚至持续数年。临床主要表现为频繁的感染。
针对B 细胞缺乏症/低丙种球蛋白血症的处理策略为静脉滴注人免疫球蛋白(5 g×3天,静滴)替代治疗。输注频次:CAR-T回输后1次/月,直至B细胞恢复至正常范围或CAR-T输注满6个月;高危人群持续1次/月,直至高危因素解除并且球蛋白水平恢复正常;针对IgG≤400 mg/dl伴严重感染、持续感染或反复感染的高危人群,注意定期监测血清IgG、IgM、IgA 及外周血中CD19+或CD20+B细胞数等。
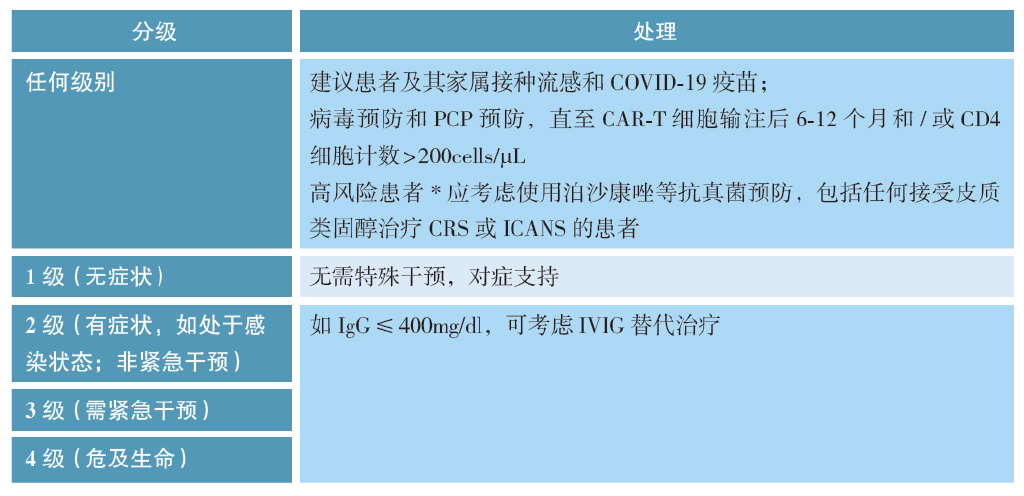
07.感染
CAR-T细胞治疗后各种类型感染发生率约为55%,其中≥3级的严重感染约为33% ;大部分感染发生在接受CAR-T细胞治疗后1~2年内,其中CAR-T细胞治疗后1个月内感染发生率可高达40%。导致感染风险增加的因素有:既往治疗的次数、近100天内的感染、糖皮质激素或托珠单抗的使用、发热性中性粒细胞减少、靶向CD22的CAR-T细胞疗法、低丙种球蛋白血症以及早期严重感染的其他潜在危险因素(包括ICANS、托珠单抗和皮质类固醇使用)。
治疗前应通过常规检查、实验室检查、病原学检查以及影像学检查进行感染筛查。目前尚无循证医学证据支持在免疫治疗同时予以常规细菌预防;需要预防的病毒感染包括HSV/VZV以及CMV、EBV、HCV;所有患者均适用氟康唑,高危患者需进行丝状真菌(霉菌)感染预防;对所有患者进行肺孢子虫预防。通过病史询问、实验室检查、病原学检查和影像学检查进行感染诊断。感染治疗原则为分级进行处理。
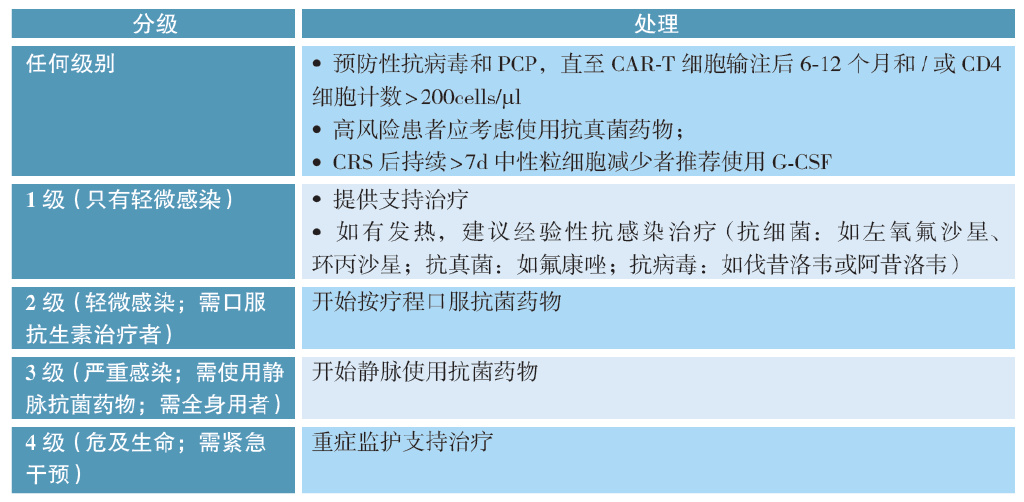
治疗期间特殊状态下感染管理建议:(1)CRS与感染鉴别:参考《CAR-T细胞治疗NHL不良作用临床管理路径指导原则》。两者临床表现有相似之处,但目前尚无特异性的标志物将两者明确区分开来;且CRS合并感染的情况时有发生,因此,对两者的发生发展的预判及干预时机把握至关重要。CRS分级与感染程度在细胞因子水平上并未显示出明显的差异。当CRS合并严重感染时,可能会出现IL-6水平的二次升高,并期望通过IL-8、IL-1β、IFN-γ三种细胞因子建立预测模型,来提高CRS与感染鉴别的特异性,但目前仍缺乏足够的临床数据。若两者无法明确鉴别,以预防性抗感染联合CRS分级治疗为指导原则。(2)特殊感染监测:包括结核、组织胞浆菌病、李斯特菌病和诺卡菌病等;注意病史询问,特别是在常规抗感染药物治疗无效时,需考虑此类特殊病原菌感染可能;(3)确诊新型冠状病毒感染患者:一般应推迟CAR-T细胞治疗,具体可参考《NCCN 癌症相关感染指南》;若由于肿瘤无法控制迫切需要进行治疗,则应根据临床医生的判断施行治疗。
08.二次肿瘤
迄今为止,患者接受CAR-T制品后的癌症发病率较低,但目前这一代病毒载体仍存在通过基因组整合或其他机制导致致癌的可能性。但基于研究样本量、随访时间及随访严谨性,目前仍无法估算CAR-T治疗后二次肿瘤发生几率,更不能完全确定CAR-T与二次肿瘤发生的直接相关性,需要更严谨的大样本病例对照研究数据。针对二次肿瘤的管理原则包括:(1)早发现、早诊断、早治疗;(2)血液肿瘤可选择新药联合治疗缓解后行异基因造血干细胞移植;(3)CAR-T治疗后规律定期复查,如PET/CT、骨髓穿刺检查、血常规、乳酸脱氢酶、肿瘤标记物等;(4)CAR-T治疗后最少随访15年,有条件者终身随访,一旦发现二次肿瘤及时上报卫健委和药监部门,进行相关病理及基因学检测。
09.过敏反应
CAR-T治疗过敏反应的诊断标准为:皮疹,多发生于细胞输注后2周内,表现为压之褪色,3~5 d可自行消退,发生原因除过敏外,可能为细胞因子释放导致毛细血管内皮脆性增加,伴或不伴有血小板减少,需结合多项指标综合评判。CAR-T治疗过敏高危人群主要为对CAR-T生产过程中的体外培养试剂、病毒载体杂质、CAR-T前未恢复的炎性背景导致的T细胞活化这几类药物过敏的人群。管理原则为:排除入组时有超敏反应的患者;在CAR-T细胞制造过程中严格控制程序和试剂;预防性使用抗过敏药物(如苯海拉明或异丙嗪)。
10.CAR-T细胞异常增殖
在CAR-T细胞回输28 d内,监测外周血CAR-T细胞体内扩增,前2周内每2~3天采集1次血样,此后每周采集1次。具体时间点为:回输后d1,d3,d5,d7,d10,d14,d21,d28。CAR-T细胞异常增殖的诊断标准为:外周血白细胞计数≥10×10⁹/L;白细胞中淋巴细胞百分比≥70%;CAR+T细胞绝对计数>600个/μL。鉴别要点包括:(1)CAR-T细胞的扩增是否与肿瘤大小的变化一致?(2)CAR-T细胞是否位于外周血以外的其他部位或在其他部位(如皮肤、肺、肝等)扩增?(3)活化的T细胞增殖失控是否由病毒感染引起?管理原则为:糖皮质激素和其他免疫抑制剂(例如抗胸腺细胞球蛋白或抗CD52抗体)。严重患者可联合使用2种或2种以上免疫抑制剂。
靶向CD19 CAR-T细胞治疗B-NHL
与2023版指南相比,2024版指南新增适应证,即将靶向CD19 CAR-T 细胞治疗作为经过二线及以上治疗[包括布鲁顿酪氨酸激酶抑制剂(BTK)抑制剂]套细胞淋巴瘤的Ⅲ级推荐。

靶向BCMA CAR-T细胞治疗MM
与2023版指南相比,2024版指南将靶向BCMA CAR-T细胞治疗既往经过至少3线治疗后进展MM的适应证由Ⅱ级推荐提升到Ⅰ级推荐。

在治疗前评估部分,2024版指南新增内容有:④本指南建议ECOG≥3分,但ECOG评分不是CAR-T治疗的绝对禁忌,尤其对于无更好治疗选择患者,临床医生可权衡患者获益及患者意愿决定是否接受治疗;⑤肾功能异常的患者可接受CAR-T细胞治疗,本指南建议,当肌酐清除率<30 ml/min时需要谨慎;CAR-T细胞治疗中,心功能不良事件发生率约26%,本指南建议左心室射血分数(LVEF)>40%,但是对于合并心肌淀粉样变性心肌淀粉样变性的患者可能表现为射血分数保留型心功能不全,即使LVEF正常,治疗中也需要更多关注;⑥临床试验显示,抗GPRC5D CAR-T可作为抗BCMA CAR-T治疗后复发或进展的挽救治疗手段之一,有条件的单位可作为备选靶点检测,不做强行要求。
在评估标准部分,2024版指南新增内容有:(1)指南建议CAR-T细胞疗效评估采用国际骨髓瘤工作组(IMWG) 标准;(2)鉴于CAR-T治疗MM时,大部分对治疗有效的患者1个月内获得骨髓微小残留病灶(MRD)转阴(流式细胞术),但免疫固定电泳转阴或轻链比例正常需要更长的时间,部分患者甚至在数月内才能达到最佳疗效;(3)推荐CAR-T细胞输注后第14、28天及后续每月进行疗效评估,直至达到最佳疗效;伴髓外病变者,建议在CAR-T治疗1个月后评估髓外病变,MRI、CT或X线片均可作为评估手段,3个月后可考虑PET-CT评估。
此外,2024版指南还新增了长期随访的内容:(1)长期随访主要包括:原发病持续缓解情况、远期毒副反应以及感染的防治。(2)随访安排:CAR-T细胞治疗后14天和28天,半年内每月评估1次,6~12月期间,每2个月评估1次;第二年每3个月进行一次全面评估,第三年及以后,每6个月或根据临床情况进行全面评估。评估的指标主要包括MM疗效的评价指标和CAR-T细胞治疗后毒副反应的检测指标。(3)维持治疗:维持治疗可能延长CAR-T治疗患者的PFS和OS,但是到目前为止,无证据级别较高的临床数据报道维持的方案、时间等,仅有个案报道免疫调节剂可能有效,但需要临床研究进一步确认。(4)复发患者的管理:目前,抗BCMA CAR-T细胞治疗后复发的挽救性治疗选择缺乏证据级别较高的临床数据,治疗可参照国内外最新指南或专家共识,包括临床试验[新药或CAR-T(如GPRC5D CAR-T)]、既往敏感的药物和未使用的新药或新的联合治疗方案。另外,经CAR-T治疗后既往无效的药物可能再次敏感。一项回顾性研究显示,非BCMA靶点的双特异性抗体及CAR-T治疗具有更高的治疗反应。
靶向CD19 CAR-T细胞治疗成人R/R B-ALL
与2023版指南相比,2024版指南将靶向CD19 CAR-T细胞治疗R/R B-ALL的适应证人群以65岁为区分,其中对于18~65岁患者的治疗由Ⅱ级推荐提升到Ⅰ级推荐。

在治疗前评估的影像学检查中新增“存在髓外病灶行PET-CT”;在治疗的回输中将回输时机改为“一般选择在清淋预处理结束后第2~7天”;在治疗后监测的CRS期实验室检查中新增“淋巴细胞亚群”Ⅱ级推荐,CAR-T动力学相关检查中新增“免疫球蛋白”Ⅰ级推荐,疗效评估中新增“其他融合基因或突变基因(限相应阳性者)”和“中枢等髓外病灶的影像学评估”Ⅰ级推荐。
需要注意的其他问题:
01
单采:单采过程中处理的全血容量需根据单采供者的绝对淋巴细胞计数(ALC) 进行判断及调整。如果ALC≥0.5×109/L,处理的目标全血量为 7~12 L;如果ALC <0.5×109/L,处理的目标全血量为12 L。单个核细胞(MNC)为CAR-T生产的关键物料,其质量对生产过程及产品质量具关键性的影响,要求采集的细胞数至少1×109 MNC。
02
单采后的桥接治疗:B-ALL为高侵袭性疾病,有可能出现疾病快速进展,对于部分疾病进展迅速的B-ALL患者,需要在单采后回输前进行桥接治疗,旨在降低疾病负荷并降低 CAR-T免疫毒性。若CAR-T制备周期内,临床医师判断患者处于稳定的低肿瘤负荷情况下可不进行桥接治疗。桥接方案应在评估患者对既往治疗反应、总体肿瘤负荷和肿瘤累及部位等后进行决策,应以不良反应最小化为原则,如MP(6-巯基嘌呤+泼尼松)方案。桥接化疗方案应充分考虑CAR-T输注时间,保障后续CAR-T回输,一般建议:CAR-T输注前4周内不使用聚乙二醇门冬酰胺酶;CAR-T输注前1周内不使用蒽环类、长春碱类、6-硫鸟嘌呤、甲氨蝶呤、阿糖胞苷、门冬酰胺酶等;CAR-T输注前3天内不使用糖皮质激素、羟基脲、酪氨酸激酶抑制剂。其他药物洗脱期建议,如CAR-T输注前1 周内不使用放疗(肺部放疗需间隔2周,CNS部位放疗需间隔8 周);CAR-T输注前1周内不使用鞘内化疗。
03
CNS 受累的情况:Brexucabtagene autoleucel 及Tisagenlecleucel产品说明书中明确指出不适用于CNS累及的情况,纳基奥仑赛临床试验中也排除了活动期CNS白血病的患者并在《纳基奥仑赛注射液临床应用指导原则(2023 年版)》的临床使用推荐中排除有严重CNS 疾病者,但已有临床研究提示CAR-T 细胞能够通过血脑屏障,并在CNS累及患者中观察到一定疗效,因此,在临床实践中需高度警惕是否有中枢浸润且根据患者个体情况,进行谨慎评估CAR-T细胞治疗是否获益。对于CNS-2级(脑脊液白细胞计数<5个/μl,可见原始淋巴细胞) 以下的患者,如临床医生考虑患者可通过CAR-T细胞治疗获益,可行CAR-T 细胞治疗(Ⅲ级推荐),同时需要高度重视ICANS 的发生并做好预防。
04
复发后管理:参加临床试验。

专家简介
张文君 教授
同济大学附属同济医院肿瘤中心副主任
同济大学血液研究所副所长
医学博士、副主任医师、副教授、副研究员、博士研究生导师
主要从事血液肿瘤免疫治疗和白血病干细胞靶向干预的基础和临床研究。作为项目负责人,主持国家自然科学基金3项,上海市科委项目和上海市申康研究型项目2项;作为项目骨干,参与科技部国家重点研发计划2项和国自然重点项目2项。先后以第一及通讯作者发表SCI论文10余篇,主编和参编著作3部,申报国家专利7项,研究成果曾获2014年上海市科技进步二等奖,入选2015年上海市优秀学科带头人“一带一”培养对象和上海市医苑新星培养计划;2018年荣获 “上海市人才发展基金”资助;2019年获“上海市优秀青年医师”荣誉称号;2021年上海市卫生系统青年人才最高荣誉奖项“银蛇奖”。