2026年3月22日-25日,第52届欧洲血液与骨髓移植学会(EBMT)年会于西班牙马德里正式召开。作为该领域最具影响力的学术会议,本届年会汇集了全球数千名专家学者,共同探讨移植与细胞治疗的最新进展。会议期间,浙江大学医学院附属第一医院黄河教授在全体大会上分享了题为“下一代装甲型与体内CARs(Armored and in vivo Next-Gen CARs)”的专题报告,系统阐述了“装甲型”与“体内生成”CAR-T两大前沿方向的技术突破与研究进展。《血液时讯》特邀黄河教授就此进行深度解读,重点探讨了这两类技术的突破性价值及其对未来细胞治疗发展路径的潜在影响。
Q1
您在本次EBMT大会上报告的主题聚焦于“装甲型”与“体内生成”这两大新一代CAR-T技术的发展方向。首先,能否请您谈谈,驱动您和团队投身于这一特定前沿领域研究的核心临床需求或科学挑战是什么?与传统的CAR-T相比,新一代CAR-T技术有望解决何种临床难题?
黄河教授:细胞免疫治疗,特别是嵌合抗原受体T细胞(CAR-T)疗法,在过去十余年间经历了从概念验证到临床应用的深刻变革。目前,全球已有十余款CAR-T产品获批,在急性淋巴细胞白血病、淋巴瘤及多发性骨髓瘤的治疗中取得了突破性疗效。然而,该领域仍面临诸多挑战,包括复发、部分亚型缓解率不足等。为应对这些挑战,下一代细胞治疗的研发主要聚焦于两大前沿方向:功能增强的装甲型CAR-T与体内(in vivo)CAR-T。
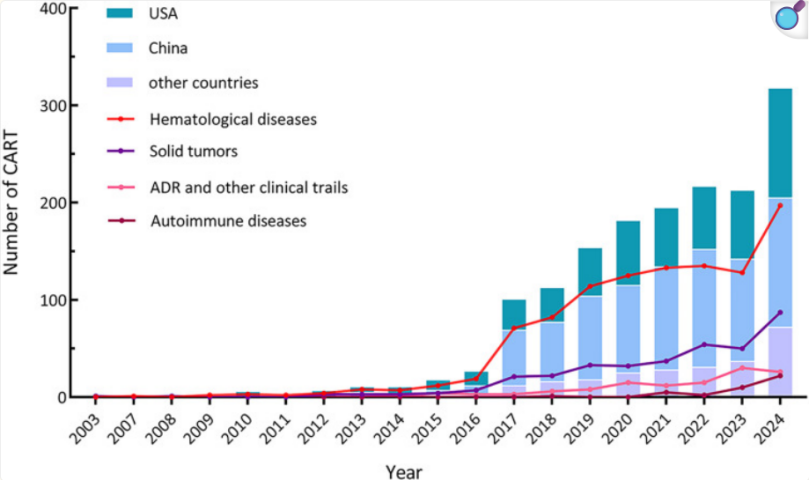
装甲型(Armored)CAR-T,旨在通过基因工程改造,使CAR-T细胞共表达具有免疫调节功能的分子,从而增强其扩增能力、持久性等功能。当前的研究热点之一是整合“代谢增强型”细胞因子,如白细胞介素-18(IL-18)或IL-10,以提升其体内效能。例如,CAR-T先驱Carl June教授团队在《新英格兰医学杂志》报道的IL-18增强型CD19 CAR-T(huCART19-IL18)在临床试验中显示出良好前景。本团队研发的表达IL-10的代谢增强型CD19 CAR-T(META10-19)的临床研究显示,仅使用传统剂量“千分之一”的极低细胞输注量,即可达到优异的临床效果。该方案不仅显著降低了细胞用量,还使部分患者免于常规的清淋处理,对自身免疫性疾病患者具有重要意义。因此,装甲型CAR-T代表了提升现有细胞疗法效能的重要发展方向。

另一项更具革命性的技术是体内CAR-T(in vivo CAR-T)。传统自体CAR-T疗法需经历淋巴细胞采集、体外激活、转导、扩增及回输等耗时数周的复杂步骤。而体内CAR-T策略则旨在通过一次体内注射,直接对患者自身的T细胞进行原位基因改造。其核心技术路径主要依赖脂质纳米颗粒或慢病毒载体,从而在体内快速生成功能性的CAR-T细胞。这项技术有望彻底规避体外制备带来的高成本、长周期和产品异质性等问题,向着“即用型”和“一针治愈”的理想治疗模式迈进。例如,华中科技大学同济医学院附属协和医院梅恒教授团队报道了利用靶向B细胞成熟抗原(BCMA)的体内CAR-T疗法(ESO-BCMA01)治疗多发性骨髓瘤的初步临床数据,展示了该路径的可行性。
综上所述,以装甲型CAR-T和体内CAR-T为代表的下一代细胞治疗技术,正在推动该领域向更高效、更安全、更可及的方向发展。中国的研究团队与国际同行一道,在这些前沿领域进行了诸多开创性探索,并持续将基础研究成果转化为具有临床价值的治疗策略,有望为更广泛的患者群体带来新的希望。
Q2
在“新一代CAR-T”专场中,您报告中提到的新型策略,在增强疗效、提升安全性或拓宽应用可及性上,带来了哪些具有前景的关键创新或实证数据?您如何看待这两种技术在临床中的定位?
黄河教授:装甲型CAR-T与体内CAR-T技术,其核心治疗范式仍基于经典的CAR-T原理:即通过基因工程手段,在患者T细胞表面表达能够特异性识别肿瘤相关抗原的嵌合抗原受体,从而引导T细胞精准杀伤靶细胞。相较于目前已上市的传统CAR-T产品,这两种新一代技术路径在制备流程、生产成本及治疗可及性方面呈现出显著的优势。
具体而言,META10-19等装甲型CAR-T因其经过工程化改造增强了体内增殖与持久性,仅需输注极低剂量的细胞即可达到有效治疗浓度。这不仅降低了对细胞数量的要求,使得从少量外周血中即可分离并制备出足量治疗细胞,也避免了传统工艺中依赖血细胞分离机进行大规模淋巴细胞采集的繁琐步骤。而对于体内CAR-T技术,其优势在于通过单次注射携带CAR基因的载体,直接在患者体内生成功能性CAR-T细胞,从而彻底规避了冗长、复杂且昂贵的体外制备过程,为实现“即用型”治疗模式提供了可能。
目前,这两类技术已在血液系统肿瘤和自身免疫性疾病的治疗探索中积累了初步的临床证据。例如,本团队参与了中国科学技术大学附属第一医院(安徽省立医院)王兴兵教授团队牵头开展的META10-19治疗急性白血病临床研究,证实了该药物的卓越疗效与良好安全性,相关研究结果已发表于《柳叶刀-血液病学》期刊。在本届EBMT年会上,我们团队则进一步报告了META10-19在B细胞淋巴瘤患者中的治疗潜力。此外,在系统性红斑狼疮等自身免疫性疾病的早期探索性治疗中,此类新型CAR-T技术同样展现出独特价值,部分患者在不进行清髓性预处理的情况下接受治疗,依然获得了良好的疗效,初步验证了其在更广泛疾病领域应用的可行性。
展望未来,新一代CAR-T技术的成熟与普及仍有赖于多中心、大样本的长期随访研究,以进一步确认其疗效的持久性、稳定性和长期安全性。随着技术迭代与临床经验的不断积累,这些创新策略有望突破现有细胞治疗的瓶颈,最终为更广泛的患者群体提供更高效、更便捷的治疗选择。

Q3
本次EBMT大会议程中,CAR-T或更广义的细胞免疫治疗领域极为突出。请问有哪些新进展、新议题或讨论热点令您印象深刻?全球学者的议题折射出该领域正朝着哪些方向加速演进?
黄河教授:造血干细胞移植历经数十年发展,已成为治疗恶性及难治性血液系统疾病的基石性手段。在精准医学时代背景下,该技术正朝着更为精细化、个体化的方向持续演进。
实现精准的临床决策是当前发展的核心。这首先体现在患者筛选与适应症的严格把握上,需综合疾病分子生物学特征、预后评分及患者全身状态进行全方位评估。其次,在预处理方案的优化中,临床实践正从传统的标准化化疗,转向探索化疗、靶向药物及免疫治疗等多种手段的联合策略。此外,在并发症的防治方面,依托对移植物抗宿主病、感染、复发等关键病理机制的深入理解,通过分子监测与靶向干预进行主动管理,已成为改善患者长期生存质量的重要途径。
值得关注的是,作为细胞治疗领域的两大支柱,造血干细胞移植与CAR-T细胞疗法如何实现优势整合与序贯应用,已成为前沿热点话题。本届EBMT年会上呈现的多项研究报告,正是围绕上述方向进行了深入探讨。综上所述,通过移植策略的持续优化,以及与CAR-T等先进治疗模式的协同探索,造血干细胞移植技术正不断拓展其内涵与外延。相信这些基于精准医学理念的临床与研究进展,将持续推动整个领域的革新,最终为患者带来更为高效且安全的治疗选择。



专家简介

黄河 教授
浙江大学医学院附属第一医院
浙江大学求是特聘教授,浙江省特级专家,主任医师,博士生导师,现任浙江大学医学院附属第一医血液科骨髓移植中心主任,浙江大学血液学研究所所长,干细胞与细胞免疫治疗浙江省工程中心主任,中华骨髓库专家委员会副主任委员,中华医学会血液学分会副主任委员,亚洲细胞治疗组织学术委员会副主席,欧洲血液与骨髓移植学会国际学术委员会委员,浙江省免疫学会理事长,主要研究方向为干细胞基础研究与造血干细胞移植临床应用、细胞免疫治疗前沿技术与转化研究先后于2003年及2015年2次荣获国家科技进步奖二等奖,作为负责人承担973 863 国家自然科学基金重点项目国家自然科学基金国际合作与交流项目等27项,以主要通讯作者在New England Journal of Medicine, Nature, Nature Medicine、Cell Research, Lancet Haematology等期刊发表SCI论文近200篇,获省部级以上科技奖项15项 ,授权发明专利21项。近5年在国际大型会议担任主席、特邀报告和口头报告百余次,主编人民卫生出版社出版的国内首部CAR-T细胞治疗学专著《CAR-T细胞免疫治疗学》,共同主编人民卫生出版社全国研究生《血液内科学》教材。任国际造血干细胞移植领域权威杂志Bone Marrow Transplantation Journal of Hematology and Oncology编委。