前言:万众期待的2026年欧洲血液与骨髓移植协会(EBMT)年会即将于3月22日在西班牙马德里开幕。其中,“非GVHD并发症”专场聚焦于造血干细胞移植(HSCT)后一系列危及生命的并发症,涵盖血栓性微血管病(TMA)、肝窦阻塞综合征/静脉闭塞性疾病(SOS/VOD)、移植物功能不良(PGF)等。本专场的研究从新型治疗药物的长期疗效、早期预测生物标志物、风险因素分析到微生物组影响等多个维度,揭示了当前的研究热点与临床管理新策略。本文将为您梳理该专场的核心口头报告内容。
本届EBMT年会"非GVHD、非感染性并发症(Non-infective complications other than GVHD)"专场呈现了移植并发症领域从机制研究到临床转化的完整进展。在血栓性微血管病方面,瑞利珠单抗的长期疗效和口服伊普可泮的真实世界数据为TA-TMA提供了更丰富的治疗选择;在肝窦阻塞综合征领域,基线肝脏弹性成像和ADC治疗后风险因素分析为个体化预防策略提供了工具;在生物标志物开发方面,PTX3和血管生成因子谱为早期识别高危患者开辟了新途径;在植入功能不良研究中,统一诊断标准的应用揭示了PTCy与免疫重建延迟的关联;而肠道菌群研究则强调了微生态在儿童移植预后中的关键作用。这些研究共同体现了精准医学在移植并发症管理中的应用趋势,通过早期识别、风险分层和靶向干预,有望进一步降低非复发死亡率,改善患者长期生存。期待马德里年会上这些研究的完整数据发布,为临床实践带来更多循证依据。以下为各项研究摘要的精要。
01
儿童HSCT-TMA:瑞利珠单抗52周长期疗效
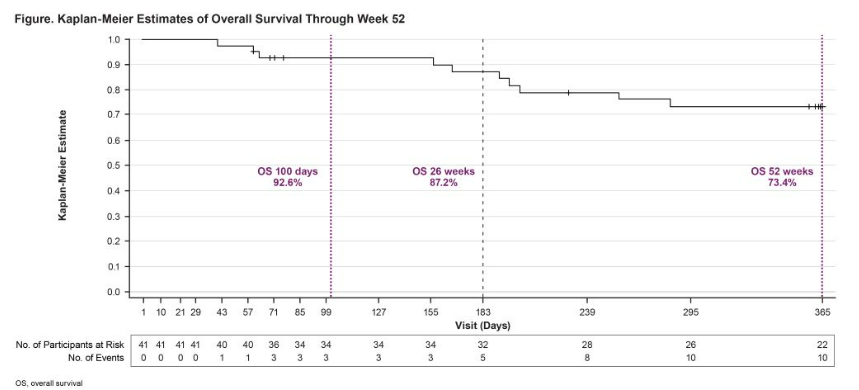
西班牙马德里拉巴斯大学医院的David Bueno-Sanchez带来了“瑞利珠单抗联合最佳支持治疗用于儿童造血干细胞移植相关血栓性微血管病的52周III期试验结果”(OS04-01)。 这项全球多中心、单臂、开放标签的III期试验(ALXN1210-TMA-314)评估了补体C5单抗瑞利珠单抗(Ravulizumab)在儿童HSCT-TMA患者中的长期疗效与安全性。41名患儿接受了为期26周、基于体重的瑞利珠单抗治疗,随后进行26周随访。至第26周,70.7%的患者达到方案定义的TMA缓解(其中完全缓解17.1%,部分缓解53.7%)。关键指标如尿蛋白肌酐比值、血小板计数和乳酸脱氢酶水平均持续改善至52周。估计的52周总生存率为73.4%。治疗期间未报告脑膜炎球菌感染,安全性可控。患者及家长报告的生活质量评分也随时间显著提高。该研究证实,瑞利珠单抗能为儿童HSCT-TMA患者带来具有临床意义的长期生存获益和持续的实验室指标改善。
02
内皮病风险预测:POEM研究序贯模型
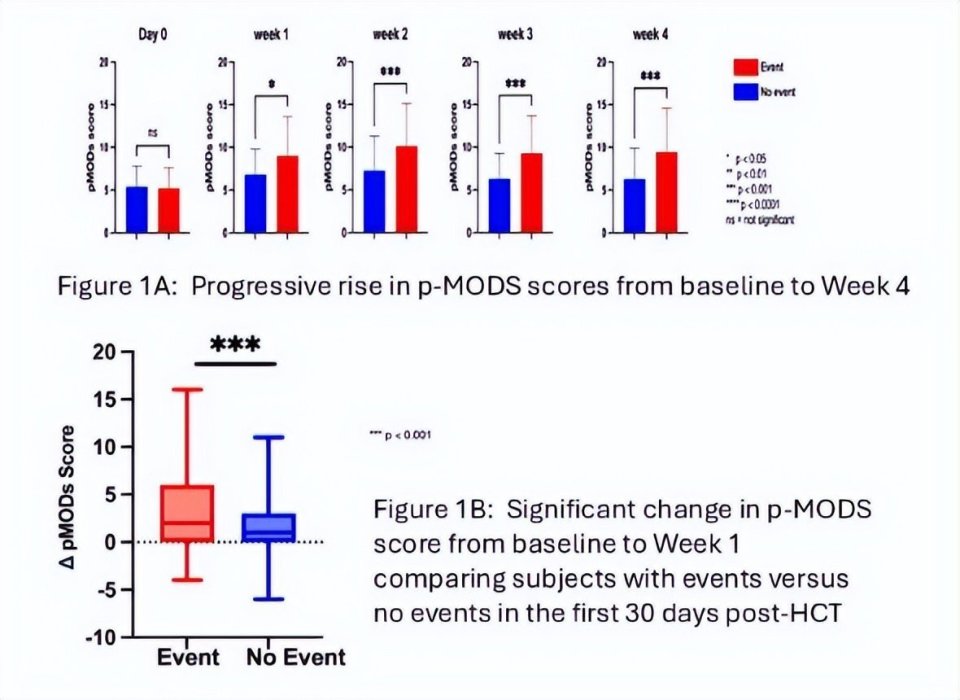
美国杜克大学的Kris Michael Mahadeo带来了“POEM多中心研究的中期更新分析:建立预测HCT后内皮病的序贯时间调整风险模型”(OS04-02)。 POEM研究是一项前瞻性多中心注册/生物样本库研究,旨在评估儿童HCT后内皮细胞损伤相关疾病,包括窦阻塞综合征(SOS)、移植相关血栓微血管病(TA-TMA)、毛细血管渗漏综合征(CLS)、弥漫性肺泡出血(DAH),及儿科多器官功能障碍综合征(p-MODS)的风险。对239名入组超过100天的受试者分析显示,内皮病总体发生率为13.4%。研究发现,在移植后第1周即出现p-MODS评分进行性升高(中位增加2分)的患者,随后30天内发生内皮病或需要重症监护支持的风险显著增加。此外,通过比较循环血管生成因子,研究发现在基线时,未来发生SOS的患者其CD31、VEGF-D、EMMPRIN和Lyve-1水平显著低于对照组,表明血管生成特征谱或许能在预处理前识别SOS高危患者,结合移植后早期的p-MODS动态评分,有望构建序贯时间调整的风险预测模型。
03
口服伊普可泮:高危TA-TMA挽救治疗
浙江大学医学院附属第一医院/良渚实验室黄河教授团队的Fei Gao带来了“口服补体因子B抑制剂伊普可泮(Iptacopan)治疗移植相关血栓性微血管病:一项多中心回顾性研究”(OS04-03)。 该研究回顾性分析了2024年7月至2025年5月期间,来自中国7个中心的27例高危TA-TMA患者使用口服补体因子B抑制剂伊普可泮的疗效。所有患者均曾接受过包括钙调磷酸酶抑制剂撤除、利妥昔单抗等多种挽救治疗,其中9例曾使用过依库珠单抗。患者接受伊普可泮(200mg,每日两次)治疗,中位治疗时间为27天。结果显示,总体缓解率达77.8%(9例完全缓解,12例部分缓解),中位起效时间为12天。值得注意的是,无论患者之前是否接受过依库珠单抗治疗,其缓解率无显著差异(未治疗组83.3% vs. 预处理组66.7%)。至末次随访,缓解者的6个月生存率显著高于无缓解者(67.9% vs. 0%)。研究表明,伊普可泮作为挽救疗法,对高危TA-TMA患者(包括依库珠单抗经治者)显示出显著的临床疗效。
04
儿童肠道菌群:粪肠球菌优势与死亡率
意大利罗马的Enrico Velardi带来了“围移植期肠道微生物组损伤与粪肠球菌优势定植与儿童异基因造血细胞移植死亡率增加相关”(OS04-04)。 这项在美国、意大利三中心开展的前瞻性纵向研究,通过鸟枪法宏基因组学分析了349名儿科allo-HCT患者的1699份粪便样本。研究发现,移植后肠道微生物组的α多样性显著下降,总细菌载量减少约五倍。移植后第28天,97%的患者出现分类单元优势定植(相对丰度≥30%),其中肠球菌最为常见。多变量分析显示,恶性疾病和使用哌拉西林/他唑巴坦预防与肠球菌优势定植和丰度增加相关。重要的是,在移植后早期(植入期间),更高的肠道微生物组α多样性预示着更低的全因死亡率风险。通过生物信息学工具FLORAL分析,研究进一步将粪肠球菌鉴定为与死亡率正相关的关键菌种。这支持了围移植期微生物组特征对预后的重要性。
05
基线肝脏弹性成像:SOS/VOD风险预测
意大利米兰的Lorenzo Lazzari带来了“基线肝脏弹性成像预测异基因造血干细胞移植患者发生SOS/VOD的风险”(OS04-05)。 该单中心回顾性研究纳入了446名在移植前至少接受过一次肝脏瞬时弹性成像(TE)评估的成人alloHCT患者,旨在评估基线TE值对SOS/VOD的预测价值。结果显示,发生SOS/VOD的患者其基线TE值(10.3 kPa)显著高于未发生者(6.2 kPa)。时间依赖的ROC曲线确定7.9 kPa为最佳阈值。基线TE值升高的患者,其100天SOS/VOD累积发生率(13.8% vs. 2.8%)和1年非复发死亡率(19.8% vs. 13.3%)均显著更高。线性回归证实基线TE是SOS/VOD的独立阳性预测因子。研究表明,基线TE测量是一种有效的无创工具,可用于识别alloHCT后SOS/VOD高危患者,尤其是那些曾暴露于奥加伊妥珠单抗:等肝毒性药物的患者,从而可能受益于针对性的预防策略。
06
正五聚蛋白3:GVHD和TRM早期生物标志物
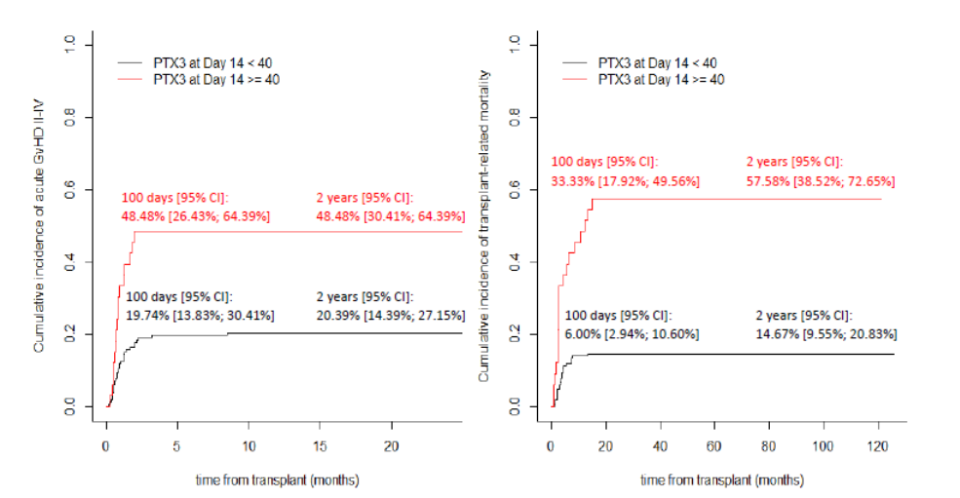
意大利米兰的Rosamaria Nitti带来了“Pentraxin 3作为预测急性移植物抗宿主病和移植相关死亡率的早期生物标志物”(OS04-06)。 这项前瞻性多中心观察性研究评估了血浆正五聚蛋白3(PTX3)在预测allo-HSCT主要结局中的价值。对207名连续患者的分析发现,移植后第14天(D+14)的PTX3水平是预测急性GVHD II-IV级和移植相关死亡率(TRM)的关键时间点。PTX3浓度越高,发生急性GVHD II-IV级和TRM的风险越高。研究者确定了D+14血浆PTX3 40 ng/ml作为cut-off值。高于此值的患者,其100天急性GVHD II-IV级累积发生率、100天及2年TRM均显著更高。在多变量Fine-Gray回归模型中,D+14的PTX3浓度是预测此后发生急性GVHD II-IV级和TRM风险的唯一保留变量。该研究证实,移植后D+14的血浆PTX3水平是识别急性GVHD和TRM高危患者的有价值生物标志物。
07
植入功能不良:PTCy与免疫重建延迟
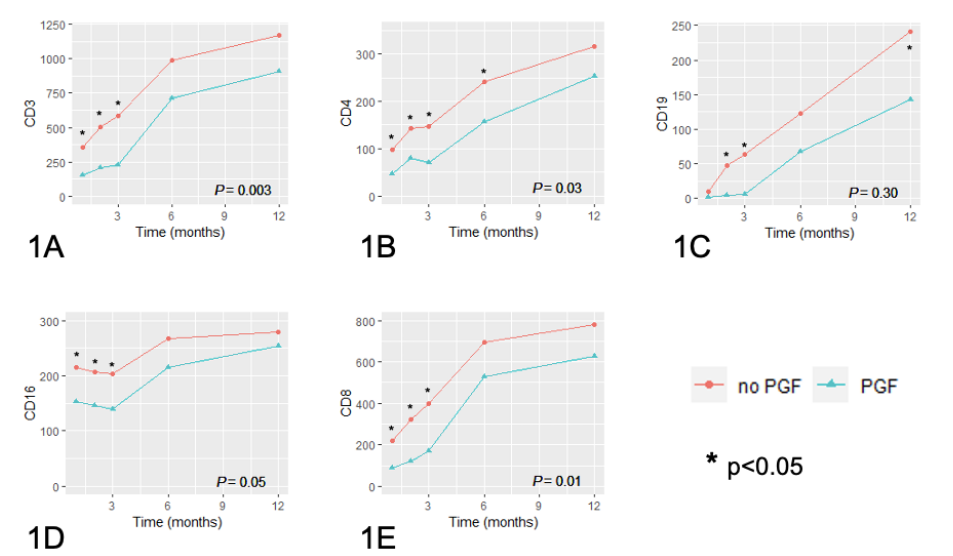
意大利贝尔加莫的Davide Murgia带来了“应用2024年统一定义分析造血干细胞移植后不良移植物功能:发病率、危险因素及结局”(OS04-07)。 该单中心回顾性研究首次应用2024年国际统一标准,评估了2015-2025年间655名成人HSCT患者中不良移植物功能(PGF)的发病率、风险因素和临床结局。PGF的累积发病率为7%。多变量分析显示,骨髓纤维化、骨髓增生异常综合征、主要ABO血型不合、CD34+细胞剂量<5x10⁶ cells/kg以及使用移植后环磷酰胺(PTCy)是PGF的独立相关因素。PGF患者具有更高的5年非复发死亡率(25% vs. 15%),且其主要死因为感染。PGF患者还表现出显著的免疫重建延迟,包括T细胞和B细胞恢复受损。ROC分析发现移植后第30天CD3+计数<178/μL是预测PGF的最佳早期指标。在治疗方面,艾曲波帕和干细胞回输对管理PGF显示出疗效。
08
ADC治疗后VOD:急性白血病移植风险因素
俄罗斯圣彼得堡巴甫洛夫大学Gorbacheva研究所的Zhemal Rakhmanova带来了“抗体药物偶联物治疗后接受异基因造血干细胞移植的急性白血病患者发生肝静脉闭塞病的风险因素”(OS04-08)。 该研究回顾性分析了121例在ADC——吉妥珠单抗奥唑米星(gemtuzumab ozogamicin)/奥加伊妥珠单抗治疗后,接受allo-HSCT的急性白血病患者,旨在确定VOD/SOS的风险因素。根据EBMT标准,VOD发生率为30%(36/121),中位发生时间为移植后14天,且VOD组患者的100天非复发死亡率显著更高(42% vs. 5%)。单变量分析显示,晚期疾病状态、使用含钙调磷酸酶抑制剂的方案(对比无钙调磷酸酶抑制剂方案)、儿童亚组中使用白消安为基础的预处理方案以及移植前EASIX评分>3是VOD的显著风险因素。然而,在多变量逻辑回归模型中,只有移植时处于晚期疾病状态是VOD的独立预测因素,使用含钙调磷酸酶抑制剂的方案仅显示出显著性趋势。研究表明,对于移植前接受过ADC治疗的患者,晚期疾病状态是VOD的关键风险因素。
总 结
本次OS04专场全面展示了HSCT后非GVHD并发症领域从前沿治疗到精准管理的最新进展。在治疗方面,补体抑制疗法依然是TA-TMA的研究核心,无论是C5抑制剂瑞利珠单抗在儿童中的52周长期数据,还是新型口服补体因子B抑制剂伊普可泮在难治性患者中显示出的高缓解率,都为此类致死性并发症提供了强有力的武器。在预测与风险分层上,研究愈发深入和精准:基线肝脏弹性成像(TE)和移植前血管生成因子谱(如CD31, VEGF-D)有望无创识别SOS/VOD高危患者;移植后D+14的PTX3水平成为预测急性GVHD和TRM的新型血液生物标志物;而首个基于国际统一标准的PGF研究,则明确了其与免疫重建延迟、感染相关NRM的关联及特定风险因素。此外,大规模儿科微生物组研究证实了粪肠球菌优势定植与死亡率的相关性,为干预提供了新靶点。对ADC治疗后患者VOD风险的分析则提示,疾病状态是比特定药物暴露更关键的独立风险因素。这些研究成果共同指向一个更个体化、更主动的并发症管理新时代,通过早期识别高危患者、应用新型靶向药物和干预微生物生态,有望最终改善移植患者的生存与生活质量。