T细胞淋巴瘤包括T淋巴母细胞淋巴瘤/白血病和成熟T细胞淋巴瘤,侵袭性高,治疗困难。如果一线治疗无法达到缓解或原发耐药,进展到复发/难治阶段,新的药物治疗进展有限,预后很差。对于再次诱导治疗无法达到完全缓解的患者,异基因造血干细胞移植(allo-HSCT)的挽救治疗复发率高,长期生存不容乐观。近年来,随着嵌合抗原受体T(CAR-T)细胞治疗在B细胞淋巴瘤中的应用日益成熟,靶向CD7的CAR-T细胞治疗应用于复发/难治T细胞淋巴瘤的临床研究也日益增多。前期的研究显示了CD7 CAR-T治疗的短期高缓解率,但同时也发现治疗后合并长时间的骨髓抑制毒性增加了感染等并发症,使得一些患者没有条件桥接allo-HSCT。那么,如何在保证CD7 CAR-T细胞治疗高缓解率的同时降低后期骨髓抑制的毒性反应?这是摆在淋巴瘤医生面前的一个亟待研究的临床问题。
近期,北京高博医院淋巴瘤骨髓瘤科胡凯教授团队的杨帆医生在Blood Cancer Journal杂志发表了一篇题为“Low-dose CD7 chimeric antigen receptor T cells for relapsed/refractory T-cell lymphomas: a single-arm, open-label, phase Ia/Ib study”的论文,总结了团队探索的低剂量CD7 CAR-T治疗复发/难治T细胞淋巴瘤的I期临床研究和长期随访结果,为各位专家学者提供了新的思路。
研究背景
胡凯教授谈到:复发/难治T细胞淋巴瘤患者的治疗很棘手,需再次诱导达到缓解后行allo-HSCT才能达到延长生存和治愈的目的。但这部分患者往往对化疗高度耐药,病情危重,肿瘤负荷高,合并感染等并发症发生率高,如果没有有效的诱导缓解手段,基本没有条件行allo-HSCT。临床前及早期的临床研究均证实了CD7 CAR-T细胞治疗的早期高缓解率,但也都发现治疗后长时间的骨髓造血抑制。为此,我们团队设计完成了Ia期剂量爬坡和Ib期剂量拓展的临床试验,通过降低回输CD7 CAR-T细胞的剂量,旨在探索小剂量CD7 CAR-T细胞治疗的临床疗效及不良反应。我们此次同时报告了2年研究随访的数据。
本研究共纳入40例高度复杂难治的患者(中位年龄:32岁;年龄范围:18-72岁)。其中35例T淋巴母细胞白血病/淋巴瘤,5例成熟 T细胞淋巴瘤。既往治疗中位线数为3次(范围:2-4),22例(55%)曾接受过造血干细胞移植(17例接受过allo-HSCT,5例接受过自体造血干细胞移植)。骨髓原始细胞比例>25%的患者占27.5%,中枢神经系统受累占25%。Ia期采用3+3的剂量爬坡模式,三个剂量组分别为1×10⁴, 5×10⁴和1×10⁵ (±30%) CAR-T cells/kg。9例患者均未出现DLT。Ib期31例患者采用1×10⁵ ( ± 30%) CAR-T cells/kg作为拓展剂量。
研究亮点
01、低剂量CD7 CAR-T体内扩增良好,不良反应可控;血细胞减少值得关注
CD7 CAR-T细胞扩增显著,流式细胞检测(图1A)中位峰值出现在输注后14天(7-30天),外周血计数中位数为82.1×10⁶/L(0.643-734)。CAR转基因通过PCR检测可持续至第396天(图1B)。10例中枢神经系统受累患者中有7例在脑脊液中可检测到CAR基因拷贝(图1C)。在治疗疗效或CAR-T细胞来源(自体或供者)方面,扩增情况未见差异。
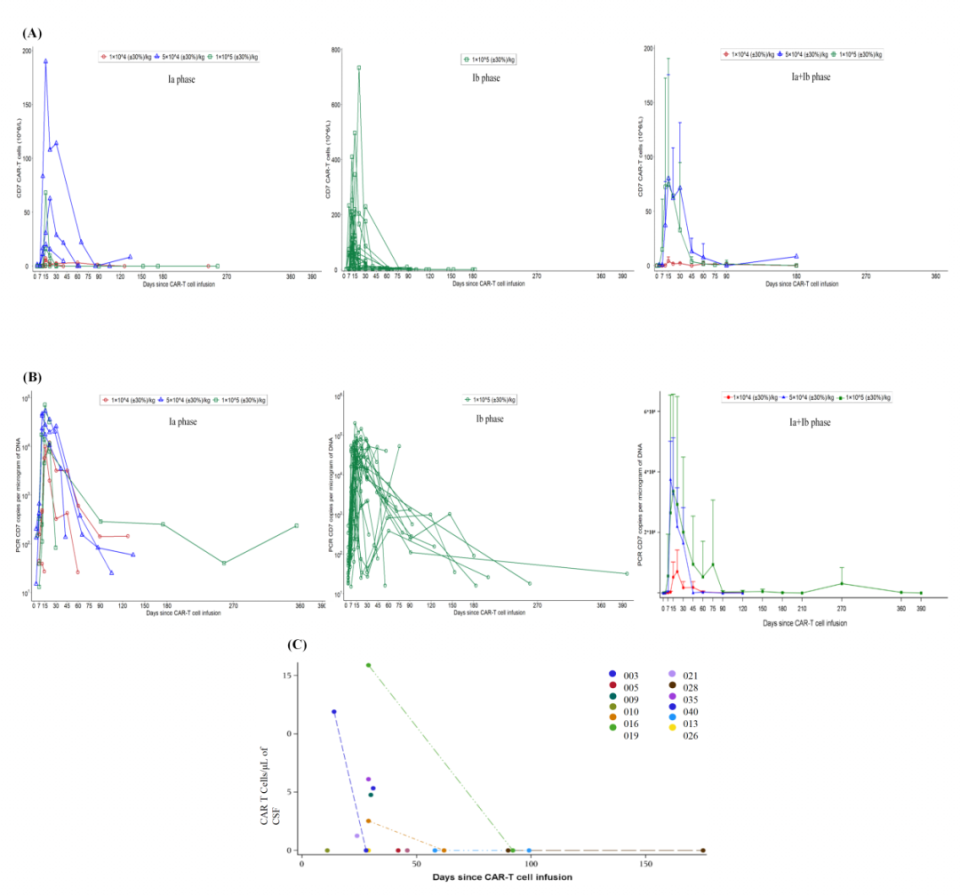
图1
CRS的发生率为92.5%,仅2例为3级CRS;2例发生ICANS(Gr1级和Gr4级)。最常见的不良反应为血液学毒性:Gr≥3级中性粒细胞减少症(97.5%,39/40)和血小板减少症(85%,34/40)。部分供者CD7 CAR-T血象延迟恢复的患者在回输了供者纯化CD34+细胞成功促进了造血恢复。30%(12/40)患者在30天内发生感染,7例为3级感染。既往接受过 HSCT 治疗的患者中aGVHD发生率为23.5%(4/17),均为1级。cGVHD发生率为30.8%(4/13),其中包含1例3级广泛型cGVHD。
02、低剂量CD7 CAR-T细胞治疗缓解率高,针对结外病变及中枢侵犯的患者均有效
在所有剂量组中,总体缓解率(ORR)为92.5%(37/40),完全缓解(CR)率为77.5%(31/40)。在Ib期队列(n=31)中,ORR 93.5%(29/31),CR 80.6%(25/31)。5例成熟T细胞淋巴瘤全部有效,其中2例PR,3例CR。在接受供体来源CAR-T细胞治疗的17例 HSCT 后复发患者中,ORR 达100%(14例CR,3例PR)。结外亚组缓解率90.6%(29/32),中枢神经系统受累亚组缓解率100%(6/6),均保持较高水平。
03、低剂量CD7 CAR-T细胞治疗诱导缓解后桥接allo-HSCT明显延长生存
中位随访30个月期间(14-58个月),治疗有效者的中位PFS和OS分别为7.05个月(95% CI:3.42-NE)和16.34个月(95% CI:4.47-NE)。两年PFS和OS分别为40.1%(95% CI:22.2-57.5%)和36.9%(95% CI:20.0-53.9%)。在CD7 CAR-T诱导缓解后桥接allo-HSCT的两年OS率[54.1%(95% CI:26.7-75.2)]显著优于未接受治疗组(n=13)[23.1%(95% CI:5.6-47.5)](P=0.038),两年 PFS [54.1%(95% CI:26.7-75.2)]也显著优于对照组[23.1%(95% CI:5.6-47.5)](P=0.063)。与非 HSCT 组相比,allo-HSCT组两年累积复发率显示出较低趋势(25.5% vs. 64.3%,P=0.149)。对11例复发患者重新穿刺评估肿瘤表面抗原分析显示,4例仍为CD7阳性,2例表现为低CD7表达,5例出现CD7阴性复发。脱靶可能是肿瘤复发的主要原因。
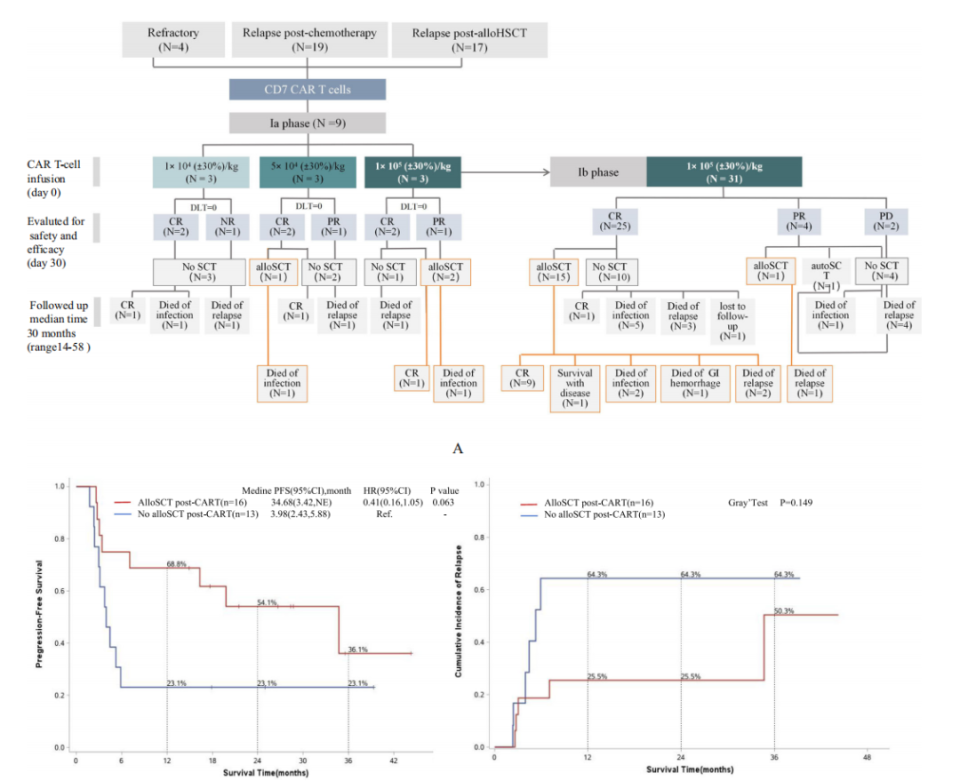
图2
我们研究显示:复发/难治性T细胞淋巴瘤应用低剂量CD7 CAR-T细胞疗法可获得高缓解率且毒性反应可控。治疗有效后桥接allo-HSCT治疗可显著提高生存率。
总结及展望
胡凯教授指出,CD7 CAR-T治疗复发/难治T细胞淋巴瘤,回输剂量在1×10⁵ ( ± 30%) CAR-T cells/kg水平即可达到显著疗效。同时我们也观察到虽然CD7 CAR-T短期缓解率高,后期需桥接allo-HSCT可明显降低复发率,延长生存。对于CD7 CAR-T治疗T细胞淋巴瘤的研究还有很多问题亟待解决,如我们观察到有3例患者检测到CD7 CAR-T的体内扩增但治疗无效,需进一步探索CAR-T的原发耐药机制;另外,CD7抗原的靶向清除对B淋巴细胞、T淋巴细胞及 NK 细胞亚群的长期免疫学影响仍不明确,需进一步总结;此外,allo-HSCT后复发的T细胞淋巴瘤患者行供者CD7 CAR-T治疗后的血液学毒性更加突出,这一部分患者后期的支持治疗或二次移植时机的选择仍需进一步研究。
北京高博医院淋巴瘤骨髓瘤科近年来积累了丰富的淋巴瘤CAR-T治疗经验,随着真实世界中CAR-T治疗的病例逐步增多,面临的临床问题更加复杂。选择合适的CAR-T治疗时机,探索个性化、精细化、全程化的管理,仍然是血液肿瘤领域未来主要的临床任务。未来我们可以结合临床、病理、分子、影像等整合诊断技术来更早了解对常规治疗无效但可从精准化CAR-T治疗中获益的患者群体,并且可通过监测ctDNA等方式提早发现复发倾向,抢先治疗,从而延长患者生存。
专家简介

胡凯 教授
北京高博医院
主任医师,医学博士,北京高博医院淋巴瘤骨髓瘤科主任
从事血液肿瘤科工作20余年,2019至今任淋巴瘤骨髓瘤科科主任,专业方向为血液系统恶性肿瘤如白血病、淋巴瘤及多发性骨髓瘤的标准化诊治,主攻免疫治疗(CAR-T细胞治疗,抗体及靶向免疫治疗等);擅长综合规范化治疗、细胞免疫治疗、抗体类药物及分子靶向治疗、自体/异体造血干细胞移植及生物治疗的综合应用,以及自体/异体造血干细胞移植治疗血液系统恶性肿瘤及移植后合并症的诊治,已有千例以上免疫治疗淋巴瘤及骨髓瘤的临床经验;其中,CAR-T细胞治疗复发/难治大B细胞淋巴瘤、T细胞淋巴瘤、中枢神经系统淋巴瘤、多发性骨髓瘤及CD19 CAR-T治疗失败后的探索性研究发表SCI论文40余篇,累计影响因子100分左右;其中,序贯二次CAR-T治疗、CAR-T联合ASCT治疗及异体CART结合异体造血干细胞移植治疗淋巴瘤及骨髓瘤更为国际领先模式,得到国内外学者广泛关注及认可。深耕临床的同时,作为主要研究者开展临床试验(IND及IIT)近40项,共参研100余项。团队的各项研究成果多次在ASH(美国血液学年会)、EHA(欧洲血液学年会)、EBMT做了大会发言,并代表国内顶尖学者成为EBMT成员。拥有科研专利一项(专利号:201420394032X),参编参译著作7本,主编3本。在多个学术团体任职。
学术任职:
中国老年学学会老年肿瘤专业委员会委员;
中国抗癌协会血液肿瘤专业委员会第一届中国T细胞淋巴瘤工作组委员;
中国健康管理协会健康科普专业委员会委员;
中国医药教育协会造血干细胞移植及细胞治疗专业委员会委员;
北京建促会血液肿瘤精准诊疗专家委员会主任委员;
北京医学会市级“枢纽型”社会组织专家委员;
北京围手术期医学研究会血液专业委员会委员;
北京肿瘤协会临床研究专业委员会委员;
北京市医学会血液委员会青年委员

杨帆
北京高博医院
副主任医师,医学硕士,北京高博医院淋巴瘤骨髓瘤科副主任
从事血液科工作近20年,专业方向为复发难治白血病、淋巴瘤、多发性骨髓瘤的CAR-T治疗及造血干细胞移植治疗,及移植后合并症的诊治。近年多次在ASH(美国血液学年会)、EBMT(欧洲移植学会)、EHA(欧洲血液学年会)、APBMT(亚太地区血液学年后)、淋巴瘤骨髓瘤免疫与靶向治疗国际高峰论坛、中国女医师协会血液学专委会分会大会均做了大会发言,代表团队在国际大会做壁报展示20余次,得到国内外广泛关注及认可。参写SCI文章20余篇,任新版《淋巴瘤靶向及免疫治疗手册》副主编。对难治/复发白血病、淋巴瘤患者的治疗有独到见解,对处理CAR-T细胞免疫治疗、移植后急、慢性移植物抗宿主病、VOD、TMA、PTLD、感染、复发、CART后CRS及ICANS等并发症有丰富经验。
学术任职:
中国女医师协会第一届靶向专业委员会常委
北京建促会血液肿瘤精准诊疗专家委员会秘书长
北京癌症防治学会淋巴瘤免疫治疗专业委员会委员;
北京癌症防治学会血液病工作委员会红细胞疾病专委会委员
中国女医师协会第一届血液专业委员会委员
中国女医师协会血液淋巴专委会委员
中国女医师协会血液学专委会白血病学组委员
中国女医师协会血液学专委会多发性骨髓瘤及相关疾病专业学组委员
高博医疗集团成人淋巴瘤(秘书)、免疫治疗、造血干细胞移植专委会委员