2025年3月30日至4月2日,第51届欧洲血液与骨髓移植学会年会(EBMT 2025)在“文艺复兴的摇篮”意大利佛罗伦萨盛大举行。作为血液学领域极具影响力的国际盛会,本届大会吸引了全球五千余名专家学者参与,共同探讨造血干细胞移植与细胞治疗的前沿进展。慢性移植物抗宿主病(cGVHD)作为异基因造血干细胞移植(alloHSCT)后的主要并发症,其研究进展成为会议焦点之一。《肿瘤瞭望-血液时讯》特邀中国人民解放军联勤保障部队第920医院血液科王三斌教授,对其中的两项关键研究进行深入点评,以期为临床实践或未来研究提供借鉴。

01
ORCA-T®在预防cGVHD方面优于传统异基因移植:一项针对晚期血液恶性肿瘤的随机3期试验(摘要号:0S15-01)
背景
尽管采用多种药物预防,移植物抗宿主病(GVHD)仍是异基因造血干细胞移植(alloHSCT)后的主要治疗相关并发症。Orca-T是一种正在研究中的异基因T细胞免疫疗法,利用高纯度调节性T细胞预防GVHD。我们报告了Precision-T研究中随机3期部分的结果,该研究比较了Orca-T与传统异基因移植[使用他克莫司/甲氨蝶呤(Tac/MTX)](NCT05316701)。
方法
纳入18-65岁,处于完全缓解(CR)状态,接受清髓性alloHSCT治疗的中高危急性白血病,或骨髓原始细胞≤10%的高危骨髓增生异常综合征(MDS)成人患者,接受HLA匹配供者移植,按1:1随机分配接受Orca-T联合单药Tac或未处理的外周血干细胞联合Tac/MTX。主要终点是无中重度cGVHD的生存率(cGFS)。采用意向治疗(ITT)原则进行分析。
结果
随机人群包括93例Orca-T患者和94例Tac/MTX患者,中位年龄43.5岁(范围19至65岁),56%为男性,73%为白人。原发疾病包括急性白血病(53%髓系,30%淋巴系,3%混合表型)和高危MDS(14%)。供者为8/8 HLA匹配(53%为兄弟姐妹,47%为无关供者)。Orca-T在集中GMP设施中生产、分发,并在美国19个中心成功输注给88例患者。截至数据截止时,5例随机分配至Orca-T的患者因与制造无关的原因未接受Orca-T。
与Tac/MTX相比,Orca-T的cGFS显著更高(HR 0.26;95% CI:0.14~0.47,P<0.00001)。在ITT人群中,Orca-T组和Tac/MTX组患者1年cGFS率分别为78%(95%CI:65%~87%)和38%(95% CI:26%~51%)。1年时中重度cGVHD的累积发生率分别为13%(95% CI:5%~23%)和44%(95% CI:31%~56%)(P<0.0003)。1年总生存率(OS)分别为94%(95% CI:86%~97%)和83%(95% CI:73%~90%)(HR 0.49;95% CI:0.20~1.22;P=0.12)。
Orca-T组和Tac/MTX组1年无复发生存率分别为76%和74%(HR 0.80,P=0.49)。两组所有患者均成功植入。两组分别有43%和51%的患者出现常见不良事件评价标准(CTCAE)≥3级感染,而7%和13%的患者出现≥3级急性GVHD(aGVHD)。1年时非复发死亡的累积发生率分别为4%和14%。
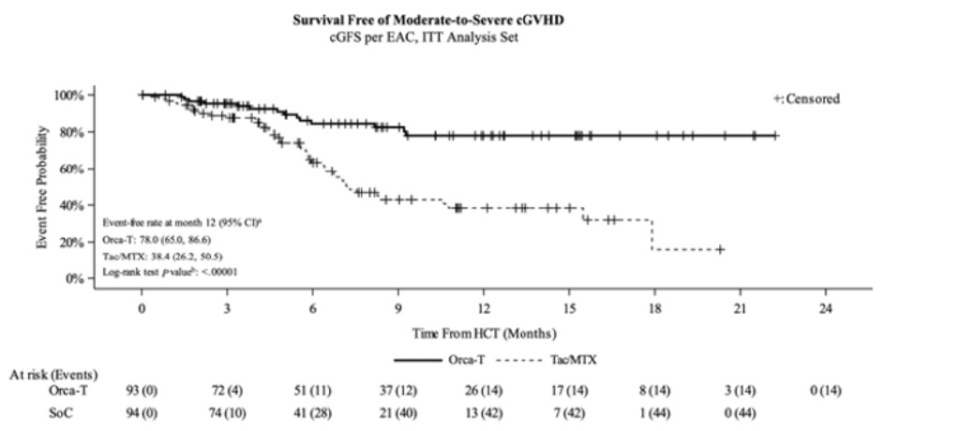
结论
该随机3期试验达到了主要终点,证明与Tac/MTX相比,Orca-T的cGFS更高,这主要归因于显著减少的cGVHD和总生存率的积极趋势。结果表明,Orca-T可被视为接受HLA匹配供者移植的血液恶性肿瘤患者在清髓性预处理后的新治疗标准。
专家点评
王三斌教授:GVHD仍然是alloHSCT后的主要并发症之一,严重影响患者的生存率和生活质量。Orca-T是一种来源于供者的高度纯化的调节性T细胞。Precision-T研究是一项随机、开放标签的3期临床试验,旨在比较Orca-T与传统alloHSCT(使用他克莫司/甲氨蝶呤)在预防cGVHD方面的效果。
研究纳入处于CR状态的中、高危急性白血病,或骨髓原始细胞≤10%的高危MDS成人患者,接受HLA全合血缘或非血缘供者移植。共187例患者按1:1随机分组。
结果表明Orca-T组的cGFS(无cGVHD生存率)显著高于传统组,1年cGFS率分别为78%和38%,中重度cGVHD的累积发生率分别为13%和44%。此外,Orca-T组的1年OS率为94%,高于传统组的83%。在1年无复发生存率方面两组相似。在CTCAE≥3级感染和≥3级aGVHD的发生率方面,与传统组相比Orca-T组也有下降趋势。
综上所述,该随机3期试验达到了主要终点,证明与传统组相比,Orca-T的cGFS更高。Orca-T的成功,为GVHD的预防开辟了新的途径,未来有望在更广泛的患者群体中应用,进一步降低GVHD的发生率,提高移植治疗的成功率和患者的生活质量。
02
患者报告的反应捕捉了cGVHD临床获益的独特维度:REACH3试验分析(摘要号:0S15-03)
背景
美国国立卫生研究院(NIH)的治疗反应标准客观描述了临床试验中的治疗结果,但可能未能完全捕捉到患者体验到的获益。此前使用国家cGVHD联盟的观察数据对患者报告的反应进行了研究。为了进一步探讨这一问题,我们现在使用注册3期试验[REACH3,芦可替尼vs.最佳可用疗法(BAT)对既往1-2线治疗失败cGVHD患者的疗效]的前瞻性数据来描述患者报告的反应[根据患者整体印象变化量表(PGIC)评估]的特征。本研究旨在评估患者报告的反应与NIH总体反应和6个月时总症状评分(TSS)反应之间的相关性,并评估从6个月时开始的无失败生存(FFS)。
方法
这项分析纳入了具有6个月PGIC数据的患者,这些数据被分为两类:(1)改善,PGIC有点改善到显著改善;(2)未改善,PGIC无变化到显著恶化。评估总体反应(根据2014年NIH标准的完全或部分反应)、TSS反应(根据改良LSS量表,cGVHD TSS减少≥7分)、FFS和总生存率(OS)。使用κ值和阳性/阴性百分比一致性(PPA/NPA)来评估相关性;基于6个月时间点的分析,Kaplan-Meier用于评估FFS和OS。
结果
在160例具有6个月PGIC反应的患者中,120例(75.0%)报告cGVHD改善[芦可替尼组:74/84例(88.1%);最佳可用疗法组:46/76例(60.5%)];40例(25.0%)报告无改善[芦可替尼组:10/84例(11.9%);最佳可用疗法组:30/76例(39.5%)]。各组的人口统计学特征基本相似(见下表)。
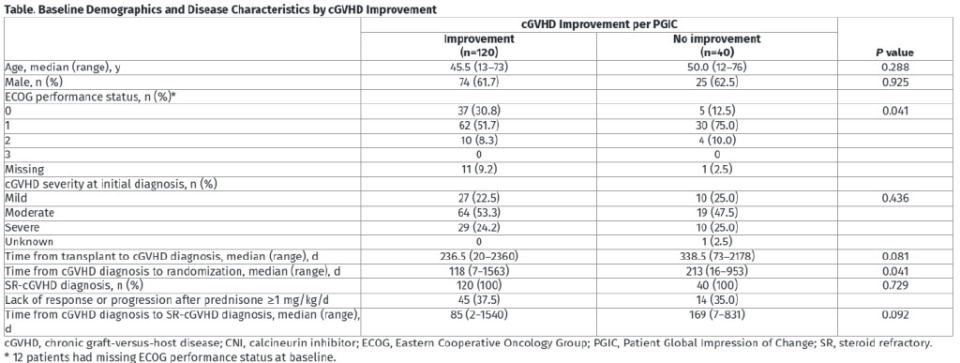
在97/160(60.6%)例具有NIH总体反应的患者中,86/97(88.7%)例报告cGVHD改善,而11/97(11.3%)例报告无改善。在63/160(39.4%)例NIH总体无反应者中,34/63(54.0%)例报告cGVHD改善,而29/63(46.0%)例报告无改善。κ值显示NIH总体反应与PGIC之间具有公平的一致性(κ=0.37;PPA=0.89;NPA=0.46;见下图)。在54/160(33.8%)例具有TSS反应的患者中,47/54(87.0%)例报告cGVHD改善,而7/54(13.0%)例报告无改善。在106/160(66.3%)例TSS无反应者中,73/106(68.9%)例报告cGVHD改善,而33/106(31.1%)例报告无改善。κ值显示TSS与PGIC之间的一致性最小(κ=0.14;PPA=0.87;NPA=0.31)。
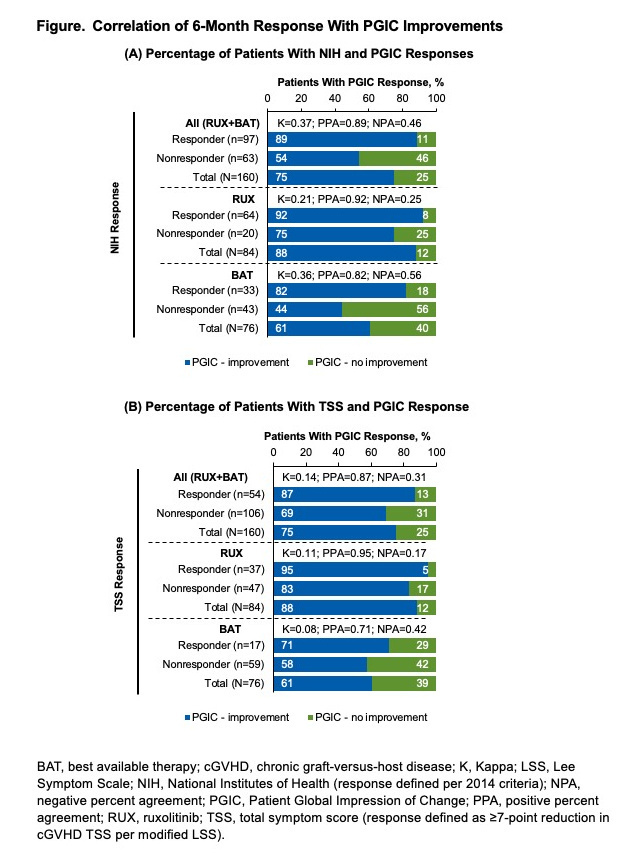
在总人群(32.9个月 vs. 0.92个月,P<0.0001)和最佳可用疗法组(18.9个月 vs. 0.03个月;P=0.002)中,报告cGVHD改善的患者与报告无改善的患者,从6个月时间点开始的中位FFS均显著更长;而芦可替尼组中,两个PGIC亚组患者中位FFS均无法评估(P=0.18)。两组之间的OS无差异。
结论
我们首次报告了一项大型随机3期cGVHD试验中的患者报告反应。研究结果进一步支持了这一结果,即患者报告的反应捕捉到了临床获益的独特维度,并且6个月时的患者报告反应与后续的FFS相关。
专家点评
王三斌教授:NIH的治疗反应标准在临床试验中能够客观描述治疗结果,但可能无法完全反映患者实际体验到的治疗获益。患者报告的治疗反应[如患者本人整体印象变化量表(PGIC)]能够提供一个独特的视角,补充传统的客观指标。
本研究首次从大规模随机3期试验REACH3中分析了患者报告的治疗反应在慢性移植物抗宿主病(cGVHD)治疗中的作用。
研究纳入了REACH3中接受芦可替尼(RUX)或最佳可用疗法(BAT)的cGVHD患者,并要求患者有6个月的PGIC数据。
研究结果表明,患者报告的治疗反应与NIH总体反应和总症状评分(TSS)反应之间存在一定的相关性,但并非完全一致。例如,尽管88.7%的NIH总体反应者报告了cGVHD改善,但仍有54.0%的非反应者也报告了改善。这表明患者报告的治疗反应能够捕捉到一些传统客观指标无法反映的治疗获益。
患者报告的cGVHD改善与更长的FFS显著相关。在整体人群中,报告改善的患者中位FFS为32.9个月,而未报告改善的患者仅为0.92个月(P<0.0001)。这表明患者报告的治疗反应可能是一个重要的预测指标。
在接受最佳可用疗法(BAT)的人群中,报告改善的患者中位FFS为18.9个月,而未报告改善的患者中位FFS仅为0.03个月(P=0.002);有趣的是,在接受芦可替尼治疗的人群中,报告改善的患者和未报告改善的患者,两者的FFS和OS没有显著差异,这可能表明患者报告的治疗反应主要与生活质量相关,而非直接影响生存。
该研究首次从大规模随机3期试验中验证了患者报告的治疗反应在cGVHD治疗中的独特价值。患者报告的治疗反应不仅与传统的客观指标相关,还能预测后续的无失败生存。这些发现支持将患者报告的治疗反应作为临床试验的重要终点之一。研究的局限性包括患者报告的治疗反应的主观性,以及不同患者对PGIC量表的理解可能存在差异。此外,研究仅限于REACH3试验的患者群体,可能需要在更大的人群中进一步验证。
专家简介

王三斌 教授
中国人民解放军联勤保障部队第920医院
主任医师、博士研究生导师
中国人民解放军联勤保障部队第920医院血液科中国医师协会血液科医师分会委员中国中西医结合学会血液学分会委员中国抗癌协会血液肿瘤专业委员会细胞治疗学组委员中国医师协会整合医学医师分会整合血液病血专业委员会委员全军医学科学技术委员会血液学专业委员会委员云南省血液学会主任委员云南省医师协会血液科医师分会副主任委员获得中国实验动物学会科学技术奖一等奖一项、云南省科技进步三等奖两项、昆明市科技计划项目一等奖一项;主持云南省省科技厅生物医药领域重大专项研究一项;在JCO、CCR等杂志以第一作者或通讯作者发表学术论文40余篇。主要工作兴趣点:(1)造血干细胞移植;(2)HIV相关血液病治疗;(3)通用型CAR-T治疗恶性血液病;(4)输血依赖型β地中海贫血基因治疗。